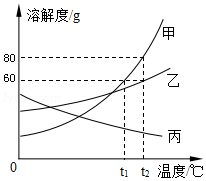
如图是甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题。
(1)0℃时,三种物质溶解度最小的是 ;
(2)t 2℃时,甲物质的溶解度是 g;
(3)将t 1℃时甲、乙、丙三种物质的饱和溶液分别升高到t 2℃,有固体析出的是 ;
(4)t 2℃时,将一定质量甲物质加到100g 水中完全溶解,再降温到t 1℃,析出甲物质15g,则t 2℃时,加入甲物质的质量为 g。
某同学用锌和稀硫酸做了如下实验,并进行相关的定量分析.将一定量的锌放入试管中,向其中加入98g质量分数为10%的稀硫酸,恰好完全反应.
(1)请计算生成氢气的质量(写出计算过程).
(2)通过已知数据还能求出的量有 (填字母,符合题意的选项都选).
a.参加反应锌的质量 b.生成硫酸锌的质量
c.稀硫酸中水的质量 d.反应后溶液中溶质质量分数.
根据不同物质的性质,提纯物质的方法可以由多种.下面呈现的是化学课堂上"物质提纯"的小组竞赛场景.
(1)甲组抽到的题目是"从30gNaCl和2gKNO 3的混合物种提纯NaCl".同学们经研究认为依据两物质的溶解度曲线,可采用如下物理方法来提纯.
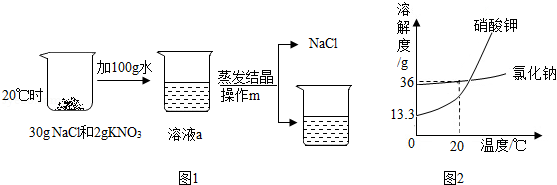
上述两固体 (填"能"或"不能")全部溶解,操作m的名称是 ,蒸发结晶后得到NaCl的质量 30g(填"大于"、"小于"或"等于").
甲组一位同学问道:"能否用降温结晶的方法从上述溶液a中析出KNO 3,从而达到分离的目的?"请你判断此方法是否可行,并说出理由 .
(2)乙组抽到的题目是"从NaCl和Na 2CO 3的混合物中提纯NaCl".同学们经过讨论认为利用两物质化学性质的差异,可采用如下化学方法来提纯.
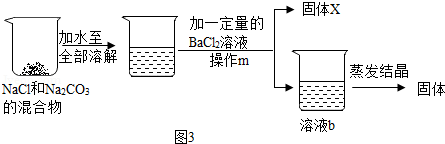
如图3中X的化学式为 .由于BaCl 2溶液的用量不易控制,会使溶液b的溶质有多种情况,导致蒸发后得到的固体可能不纯.
(3)同学们对乙组方案中溶液b的溶质成分进行探究.
【作出猜想】猜想一:NaCl、BaCl 2猜想二:NaCl 猜想三: .
【设计方案】经讨论,大家认为只用一种试剂就能作出判断.
|
实验步骤 |
实验现象 |
实验结论 |
|
取少量溶液b于试管中, 向其中加入 |
若看到 |
猜想一正确 |
|
若无明显现象 |
猜想二正确 |
|
|
若看到冒出气泡 |
猜想三正确 |
各组依据上述设计方案进行了实验,验证了反应后溶质的确有三种情况.
(4)同学们对甲乙两组提纯方法的效果进行了研讨.
【反思评价】大家认为用物理方法和化学方法都可以实现物质的提纯.用化学方法提纯还要考虑到反应物用量对提纯效果的影响.
【拓展提升】老师说:"合理选择试剂,用化学方法可以从NaCl和Na 2CO 3的混合物中提纯NaCl,方法是向混合物中加入过量的 ,充分反应后,经蒸发结晶就能得到NaCl."
炎热的夏天,在家中可以自制汽水来解暑消热。
【准备材料】1.5g小苏打、1.5g柠檬酸、蔗糖、果汁、凉开水、500mL饮料瓶
【配制流程】
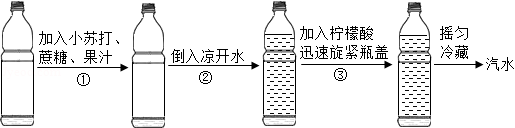
(1)下列是制汽水的操作或现象的相关问题,请选择Ⅰ或Ⅱ进行解答 。
Ⅰ.步骤②中为什么要用凉开水制汽水?
Ⅱ.步骤③旋紧瓶塞后,为什么汽水中的气泡会由多变少直至不再冒出?
(2)制汽水时,小苏打中的HCO 3 ﹣与柠檬酸溶液中的H +反应后生成的气体是 。为证明柠檬酸溶液中有H +,可以选择下列物质中的 进行验证(填字母,符合题意的选项都选)。
a.镁带 b.铜片 c.食盐 d.鸡蛋壳 e.石蕊溶液
下面是同学们制取氧气和探究氧气性质的活动.

(1)如图1是实验室制取氧气的装置,该反应的化学方程式为 ,仪器a的名称是 .操作中有很多注意事项,例如在收集氧气时看到气泡从瓶口逸出,应该 ,再将集满氧气的集气瓶正放在桌面上:实验中有些错误操作可能会使试管炸裂,写出为避免试管炸裂的一个正确操作 .
(2)如图2①中木炭在氧气中充分燃烧的化学方程式为 .反应完毕盖好玻璃片,将集气瓶倒置(如图2②),玻璃片未掉下来的原因是 .
阅读下列科普短文.
根据短文回答以下问题:
提到炸药,同学们可能会想到战争和暴力,但炸药的发明却促进了工业和经济的进步.我国是最早发明火药的国家,黑火药是我国古代的四大发明之一,主要分为硝酸钾、硫、木炭等.黑火药经点燃,发生剧烈燃烧,反应原理为:2KNO 3+S+3C K 2S+N 2↑+3CO 2↑
黑火药经阿拉伯传到欧洲,随后各国化学家陆续研制出各种炸药,如意大利化学家索布雷罗发明的硝化甘油,爆炸时威力很大,但安全性很低.瑞典化学家诺贝尔在前人研究的基础上,经过反复实验,研制出安全性很高的硝化甘油炸药,提高了它的利用价值.炸药的研发还在继续,安全烈性炸药不断问世,如TNT、黑索金等.
黑火药推动了炸药的快速发展,它虽然已退出军事领域,但依然发挥着重要的民用价值,如制造焰火、定向爆破等.我国近年来研制的纳米级黑索金,在理论和实验制备等方面获得了突破,将会继续在工业和军事领域做出贡献.
(1)黑火药不需外界提供氧气也可以发生爆炸,这是因为其成分中的 生成氧气的结果.
(2)通过阅读,下列说法正确的是 (填字母,符合题意的选项都选).
a.黑火药作为一种古老的炸药,现在已停止使用
b.黑火药能发生爆炸与它燃烧后生成气体并放出热量有关
c.使用危险物质时,我们应采取一些措施提高其安全性,更好地发挥其作用
(3)炸药属于易爆物,生活中我们有时会接触一些易爆物,下列建议正确的是 .
a.在加油加气站禁止打电话 b.夜晚发现家中燃气泄漏需要开灯检查.