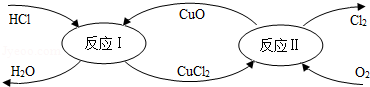
在催化剂的作用下,用O 2将HCl转化为Cl 2,可提高效益,减少污染.
(1)写出反应Ⅰ的化学方程式 ;
(2)反应Ⅱ所属基本反应类型为 ;
(3)钠在氯气中燃烧生成氯化钠,若4.6g钠完全转化为氯化钠,至少需要氯气的质量是多少?
根据下列装置图,回答问题:

(1)用高锰酸钾制取氧气,选用的发生装置是 (填序号),为防止高锰酸钾粉末进入导管,该装置需做一点改进的是 ,若用D装置收集氧气,当观察到 时,便可开始收集。
(2)实验室制取二氧化碳用选用的一组装置是 (填序号),反应的化学方程式是 ,图G是某同学利用报废试管设计的制二氧化碳的发生装置,该设计除了废物利用的优点外,请另写一个优点 。
(3)用收集的氧气完成图E铁丝燃烧的实验,集气瓶中预先放少量水的原因是 2的软塑料瓶中注入约 体积的水,立即旋紧瓶盖,振荡,观察到的现象是 。
体积的水,立即旋紧瓶盖,振荡,观察到的现象是 。
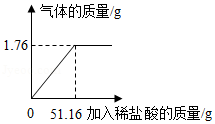
小苏打是发酵粉的主要成分之一,可用于制作发面食品。一化学兴趣小组对某小苏打样品中各成分的含量做了如下测定:将一定质量的该样品(已知杂质只含NaCl)加水全部溶解后,得到104.4g溶液,向该溶液中逐渐加入稀盐酸,产生的气体与加入稀盐酸的质量关系如图所示。试计算:
(1)m的值为 。
3与NaCl的质量比 。

娄底人在端午节有吃皮蛋的习俗。某化学小组的同学查阅资料后得知,腌制皮蛋的主要原料有:生石灰、纯碱和食盐。同学们向这三种物质中加入适量水,充分搅拌,过滤,对滤渣中溶质的成分进行探究。
小组同学讨论后一致认为,滤液中的溶质一定含有NaCl和 。(写化学式)
【提出问题】滤液中还可能含有哪些溶质呢?
【作出猜想】
2
23
223
【交流讨论】经过进一步讨论,大家认为小华的猜想不合理,原因是: 。(用化学方程式表示)
【实验探究】
|
实验操作 |
实验现象 |
实验结论 |
|
小林:取少量滤液于试管中,滴加足量的稀盐酸 |
|
小方的猜想正确 |
|
小方:取少量滤液于试管中,滴加 溶液 |
产生白色沉淀 |
小方的猜想正确 |
|
23溶液 |
无明显现象 |
小方的猜想正确 |
【交流谈论】同学们认为,通过小华的实验不足以得出其结论,原因是 。
【继续探究】小明也取少量滤液于试管中,滴加稀盐酸,却没有看到明显现象,小明对此深感疑惑。
【解释评价】经老师的指导和大家的认真思考后终于找出了原因,你认为是 。最后,老师对同学们这种严谨的科学态度给予了充分的肯定。
图甲装置是实验室常用装置,请按要求回答下列问题:
(1)请写出仪器①的名称 。
(2)实验室可用高锰酸钾制取氧气,该反应的化学方程式为 。欲用该方法制取一瓶较纯净的氧气,要选择的发生装置和收集装置是 。(填字母序号)
2,验满的方法是 。
(4)实验室在常温下用块状电石和水反应制取乙炔气体,由于该反应十分剧烈,实验必须严格控制反应速率,你认为图甲中最适宜的发生装置是 。(填字母序号)
(5)图乙所示装置具有多种用途,下列有关它的用途说法中,正确的是 。(填字母序号)
A.该装置用于排空气法收集氢气时,气体应从a端管口通入
B.瓶内装满水,用于收集氧气时,气体应从a端管口通入
2时,气体应从a端管口通入
D.瓶内装满氧气,要将氧气排出,水应从a端管口通入

某化学兴趣小组为了测定某纯碱样品(只含有Na2CO3、NaCl)中Na2CO3质量分数,取5克样品,往其中加入一定质量的稀盐酸,产生气体的质量与所加稀盐酸的质量变化如图,试计算:
(1)共产生 克二氧化碳;
(2)该纯碱样品中Na2CO3的质量分数;
(3)求恰好完全反应时所得溶液的质量分数?