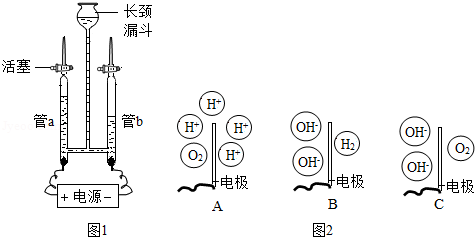
为验证水的组成元素及探究水在电极端所发生的变化,兴趣小组用如图1所示装置(夹持仪器省略)进行实验:
Ⅰ.验证水的组成元素
步骤一:向长颈漏斗中加水(含少量Na2SO4)至充满管a和管b.关闭活塞,接通电源,一段时间后关闭电源.
步骤二:检验管中气体.
(1)Na2SO4在水中能解离出 ,增强了水的导电性;
(2)电解时观察到的现象有: ;
(3)用燃着的木条分别置于玻璃管尖嘴口,打开活塞,若观察到 ,则证明气体为H2;若观察到 ,则证明气体为O2.
(4)某同学提出实验后还需检验Na2SO4的质量是否发生变化,其原因是 .
(5)若要确定水中氢、氧元素的原子个数比,需要测定 .
Ⅱ.探究水在电极端所发生的变化
步骤一:向装置中重新加水(含少量Na2SO4)至充满管a和管b,保持活塞打开,接通电源,一段时间后关闭电源.
步骤二:分别取出管a和管b电极附近的溶液,并测定溶液的pH.
(1)测定溶液pH的方法是:用玻璃棒蘸取溶液,滴到pH试纸上,把试纸显示的颜色与 ,读取pH.经测定:管a中溶液pH小于7,管b中溶液液pH大于7.
(2)管b溶液呈 性,若向溶液中加入 ,溶液变为红色,也能得出此结论.
(3)图2中能表示电解时管a中水在电极端所发生变化的结果的是 (填对应选项的字母).
化学实验是进行科学探究的重要途径。某研究性学习小组欲利用下列装置进行相关气体制取的探究,请你分析并回答问题:

(1)图中标号a的仪器名称是 。
(2)若用加热高锰酸钾固体制取并收集一集气瓶氧气,可选用的装置组合是 (填字母序号)。
(3)实验室用过氧化氢溶液和二氧化锰制取氧气的化学方程式为 。主要操作步骤有:①检查装置的气密性;②收集并验满气体;③装入药品;④组装仪器。正确的操作顺序是 (填数字序号)。
(4)F是密封良好充满空气的单气阀充气袋,现用F收集一袋较纯净的氧气,则导气管口b、c连接之前需进行的一项操作是 。
如图是某果蔬洗涤盐说明书。小明对配料表中的成分很好奇:食盐可用于杀菌消毒,为什么要加入pH调节剂,它的成分是什么?
【查阅资料】1.该品牌果蔬洗涤盐pH调节剂的成分可能是碳酸钠、碳酸氢钠、酒石酸、柠檬酸中的一种或两种。pH调节剂能维持渗透压、控制酸碱平衡。
2.大多数农药是酸性的。
3.碳酸氢钠加热易分解,碳酸钠则有较高的热稳定性,二者的溶液都显碱性。
【实验初探】取少量该固体溶于水配成溶液A。用pH试纸测得该溶液的pH=10,该洗涤盐溶液显 性,则pH调节剂中一定不含的物质是 。
【猜想与假设】该配料表中的pH调节剂可能是①碳酸钠;②碳酸氢钠;③ 。
【实验再探】
|
序号 |
实验操作 |
实验现象 |
实验结论 |
|
(1) |
取少许A溶液于试管中,滴加氯化钙溶液 |
有白色沉淀生成 |
|
|
(2) |
取适量洗涤盐,加热,将生成的气体通入澄清石灰水 |
观察到 |
证明该pH调节剂中含有碳酸氢钠。 |
【分析与结论】猜想③正确
【反思与评价】请你从1,2中任选一题回答。
1.你认为果蔬洗涤盐中pH调节剂的作用是什么? 。(答一条即可)
2.该商品配料表中有一处表述不恰当,请你改正过来 。

氧气和二氧化碳的制取和性质是初中化学的重要内容。根据下列所示的装置回答问题。

(1)请写出用A装置制取氧气的化学方程式 。若用B、C装置制取氧气,以下操作①装药品并固定装置;②检查装置气密性;③熄灭酒精灯;④加热;⑤收集气体;⑥将导气管移出水槽,正确的操作顺序是 (用序号表示)。若将红热的铁丝伸入制得的氧气中,现象是 。
(2)要制取一瓶干燥的二氧化碳,应选择的装置是 (用装置序号表示),将干燥的 分别通入G、H中,G中试纸不变色、H中试纸变红色。请用化学方程式表示H中试纸变红的原因 。
2021年12月9日,由航天员王亚平主讲的“天宫课堂”压轴实验圆满成功。实验中往漂浮在空中蓝色水球中放入半片泡腾片【主要成分是柠檬酸( )和碳酸氢钠】,泡腾片与水作用,不断产生小气泡,水球逐渐变大。产生的气泡是什么呢?为什么泡腾片遇到水才产生气泡?
【猜想与假设】
小亮同学结合已有知识,判断产生的气泡是 ,他的判断依据是 。
【设计并进行实验】
小亮同学在实验室利用以下装置,模拟用维生素C泡腾片和水制取并验证该气体的性质。

(1)仪器a的名称 ;仪器b的名称 。
(2)实验室要用以上装置制取并收集该气体。需要选择的发生装置和收集装置是 (填序号),选择此发生装置的依据是 。
(3)小亮同学将该气体通入到盛有澄清石灰水的试管中,观察到的现象是 ,请写出此反应的化学方程式 ,证明该气体是二氧化碳。
【反思交流】
小丽同学提出,泡腾片遇到其他液体也能产生气泡吗?她设计并进行了以下4个实验,将4片同样的泡腾片同时放入四个盛有50mL不同液体的烧杯中:
|
实验 |
实验现象 |
实验结论 |
|
|
实验1 |
放入水中 |
水中有大量气泡产生; |
有水存在,泡腾片才能产生 。 |
|
实验2 |
放入植物油中 |
植物油中 ; |
|
|
实验3 |
放入酒精中 |
酒精中无明显现象; |
|
|
实验4 |
放入白醋中 |
白醋中 。 |
|
设置实验1的目的是 ,通过以上实验你还得出的结论是 。
【实验启示】
维生素C泡腾片最好 保存。
酸、碱、盐是初中化学常见的化合物,研究它们的性质有重要意义。某化学探究小组设计了如下实验来探究酸、碱、盐之间的反应。

(1)实验一能观察到的现象是 。
(2)实验二体现了中和反应的实质是(以下填化学用语) 和 结合生成 。
(3)写出实验三发生反应的化学方程式 。
实验四有白色沉淀生成,对反应后的物质进行过滤后,探究小组对滤液中溶质的成分进行了实验探究。
【提出问题】滤液中溶质的成分是什么?
【猜想与假设】
(4)猜想一:氯化钠
猜想二:氯化钠和
猜想三:氯化钠和氯化钡
【实验过程】
(5)
|
实验步骤 |
实验现象 |
实验结论 |
|
取滤液少量于试管中,向其中滴入适量氯化钡溶液 |
无明显现象 |
猜想二不成立 |
|
另取滤液少量于试管中,向其中滴入适量稀硫酸 |
无明显现象 |
猜想 不成立 |
【拓展与延伸】
(6)酸、碱、盐之间在水溶液中发生的复分解反应实质上是它们解离出的离子相互结合,生成 的过程。