某工厂废液中含有CuSO 4(其他成分不含铜元素),现按以下流程回收金属铜.

(1)回收过程中,加入适量稀硫酸可除去过量铁屑,该反应的化学方程是为Fe+H 2SO 4═FeSO 4+H 2↑,这个反应所属的基本反应类型是 .
(2)洗涤后的滤渣不能用加热的方法干燥,其原因是 .
(3)现有一批废液,其中含4吨CuSO 4,理论上可从该废液中回收得到多少吨金属铜?
某未知气体X可能含有CO、CH4中的一种或两种,某同学设计实验进行探究。
查阅资料:
(ⅰ)加热时,CH4能与CuO反应生成Cu、CO2和H2O;
(ⅱ)20℃时,Ca(OH)2和Ba(OH)2溶解度分别为:0.165g,2.1g
(1)仪器M的名称是 ,CH4与CuO反应的化学方程式为 。
(2)气体X成分的猜想与探究
猜想1:只有CO 猜想2:只有CH4猜想3:既有CO又有CH4
①实验时,先往装置中通一段时间的N2,再通入气体X后加热,实验中有下列变化。
变化1:A中玻璃管内黑色粉末逐渐变红 变化2:B瓶增重 变化3:C中出现浑浊
根据变化 (填“1”“2”或“3”),可知猜想1不成立。
②根据上述变化仍无法确定气体X的成分,还需要测定 (填序号),并进行定量分析才能得出结论。
a.实验前A中CuO的质量 b.B瓶增重的质量 c.C瓶增重的质量
(3)讨论和反思
①C中用Ba(OH)2溶液而不用Ca(OH)2溶液的原因是 。
②从环保的角度,该装置还应进行的改进是 。
回答下列有关实验基本操作和设计的问题。
(1)量取18.0mL蒸馏水,最好选用的量筒规格是 (填序号)。
A 5mL B.10mL C.25mL D.100mL
(2)向如图1所示烧杯中,加入适量的 (填序号),可能引燃铜片上的白磷。
A.浓硫酸 B.硝酸铵 C.氯化钠
(3)探究紫色石蕊变色规律的实验中,往点滴板1﹣6号的孔穴中先加入如图2所示的试剂,分别滴入2滴紫色石蕊溶液。其中作为空白对照实验的是孔穴 (填孔穴编号)
(4)实验室常用较浓的过氧化氢溶液与二氧化锰制氧气。
①反应的化学方程式为 。
②实验中,为了得到平稳的气流,最适合的装置组合(如图3)是 (填序号)。
化学反应在防治环境污染中扮演了重要角色。某工厂废气中的SO2,可用以下方式处理。
方式一:2SO2+O2+2CaO═2CaSO4 方式二:2SO2+O2+4NaOH═2Na2SO4+2H2O
试计算:
(已知:CaSO4的价格为700元/吨,相对分子质量为CaSO4 136 Na2SO4 142)。
(1)CaSO4中有两种元素的质量分数呈整数倍关系,这两种元素是硫元素和 。
(2)若用方式一处理9.6tSO2,所得产品价值多少元?
(3)若用方式二处理9.6tSO2,刚好用去50t一定浓度的NaOH溶液,求所得溶液的溶质质量分数(最终结果精确到0.1%)。
(1)不同实验对反应速率有不同要求。某同学探究CO2制取实验,按要求答题。
限选控制反应速率的方法:①反应物的浓度②反应物的状态
限选试剂:A.稀盐酸B.浓盐酸C.块状石灰石D.碳酸钠溶液E.粉末状石灰石
填写下表并回答相关问题。
|
实验名称 |
控制速率的方法 |
所选用的最佳试剂 |
|
灭火器反应原理 |
① |
和D |
|
CO2的实验室制法 |
|
A和C |
写出灭火器反应原理的化学方程式 。
(2)已知:CO2和SO2既有相似性,又有差异性。
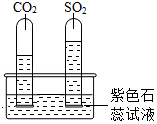
实验一:水槽中滴入紫色石蕊,将收集满两种气体的试管同时倒立于其中,片刻后实验现象如图所示,说明相同条件下的溶解性:SO2 (填“>”或“<”)CO2,试管内溶液变成 色。
实验二:已知镁条在CO2中剧烈燃烧的化学方程式为:2Mg+CO2 2MgO+C.试推测镁条在SO2中燃烧的现象为:剧烈燃烧, 。
规范使用仪器是实验成功的保障,结合如图所示玻璃仪器,回答问题。

(1)可用作热源的是 (填序号),若往仪器E中加入块状固体,则应先将该仪器 (填“平”“立”或“斜”)放。
(2)若用仪器A和D稀释浓硫酸,则D的作用是 ,若用仪器A和D进行过滤操作,还必须用到上述的一种仪器是 。(填名称)。
(3)若某气体只能用F装置收集,则该气体的密度比空气小,且 。