回答下列有关实验基本操作和设计的问题。
(1)量取18.0mL蒸馏水,最好选用的量筒规格是 (填序号)。
A 5mL B.10mL C.25mL D.100mL
(2)向如图1所示烧杯中,加入适量的 (填序号),可能引燃铜片上的白磷。
A.浓硫酸 B.硝酸铵 C.氯化钠
(3)探究紫色石蕊变色规律的实验中,往点滴板1﹣6号的孔穴中先加入如图2所示的试剂,分别滴入2滴紫色石蕊溶液。其中作为空白对照实验的是孔穴 (填孔穴编号)
(4)实验室常用较浓的过氧化氢溶液与二氧化锰制氧气。
①反应的化学方程式为 。
②实验中,为了得到平稳的气流,最适合的装置组合(如图3)是 (填序号)。
某工厂产生的废水中含有硫酸锌和少量的硫酸铜以及污泥,为了变废为宝,利用废水制取七水硫酸锌( ZnSO 4•7H 2O),其工艺流程图如下:

回答下列问题:
(1)步骤①的操作名称 .
(2)步骤②需如入过量的物质是 ,目的是 .
(3)步骤③需加入的溶液是 .
(4)步骤④的操作是蒸发浓缩, ,过滤.
(5)如果用ZnSO 4•7H 2O来配制100g 32.2%的硫酸锌溶液,需要 g七水硫酸锌.
根据下列所给信息回答:

(1)A元素的原子序数是 ,C元素在形成化合物时的常见化合价是 ,与C元素化学性质相似的是 (填字母序号,下同),属于同种元素不同微粒的是 .
(2)常温下单质为气态的是 (填化学式).
(3)在上述元素中,两元素间能形成三原子分子,此化合物常温下是一种易挥发的无色液体.试推断这种化合物的化学式并说明理由: .
某污水中除含有少量泥沙外,还含有Ca2+、Mg2+、Na+、Cl﹣、SO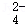 等离子,为充分利用资源,科研小组设计了如下流程回收几种离子:
等离子,为充分利用资源,科研小组设计了如下流程回收几种离子:
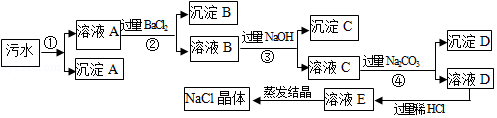
(1)①②③④步骤均有一个相同的操作步骤;此操作步骤必须用到的玻璃仪器有:烧杯、玻璃棒、 ;
(2)沉淀B的化学式为 ;
(3)加入过量稀盐酸可除去的物质有 ;
(4)步骤③中反应的方程式为 .
(1)通过初中阶段的学习,知道实验室中有多种途径可以制取氧气,如:①加热高锰酸钾②加热氯酸钾和二氧化锰的混合物 ③ .
(2)用如图所示实验装置加热高锰酸钾制氧气,下列实验步骤已按顺序排列,请你在⑦处补全还缺少的一个实验步骤.
①组装仪器 ②检查装置的气密性
③将药品装入试管 ④将试管固定在铁架台上
⑤点燃酒精灯给药品加热 ⑥收集气体
⑦ ⑧熄灭酒精灯
(3)加热高锰酸钾制氧气的装置中试管口要略向下倾斜的原因是 .
(4)用2N g的高锰酸钾加热,完全反应可制得氧气a g;如改用加热N g高锰酸钾和N g氯酸钾的混合物,完全反应可制得氧气b g;则a b(填“>、﹦或<”).

有三瓶失去标签的无色溶液,它们可能是稀HCl、稀H2SO4、Na2CO3、NaNO3、NaCl、Ba(OH)2这六种溶液中的三种.为确定它们各为何种溶液,小明做了如下实验:
(1)把它们两两混合,均无明显现象.
(2)取样,往样品中分别滴加紫色石蕊溶液.有一种溶液变红色,另一种溶液不变色,剩下的一种溶液变蓝色.能使紫色石蕊溶液变蓝色的原溶液显 (填“酸性、中性、碱性”).
(3)综合(1)(2)步实验现象及结论,可推断出这三种溶液中的一种溶液一定是Ba(OH)2溶液,还有一种溶液一定是 ;为确定剩下的另一种溶液,再取样,往其中滴加一种无色溶液,产生白色沉淀,请写出其化学方程式: .