在化学课上,老师带来一瓶未知溶液A,已知它是稀盐酸或稀硫酸中的一种,进行如下实验(图1):

观察到烧杯中的现象是(1) 。
【提出问题】A是哪一种酸?
老师要求甲、乙同学从反应后的溶液B分别展开探究。
【猜想假设】甲同学:A是稀盐酸;乙同学:A是稀硫酸。
【实验探究】(如图2)
【评价交流】甲同学的实验(2) (填"能"或"不能")得出正确结论,乙同学的实验(3) (填"能"或"不能")得出正确结论。
实验3发生反应的化学方程式为(4) ,反应后所得溶液中一定含有的离子是(5) 。
【归纳总结】通过乙同学的实验可以得出:选择试剂鉴别溶液中的待测离子时,如果待测溶液中含有干扰离子,则应在鉴别前,先另选试剂将干扰离子变成(6) 除去。经讨论我们能够总结出,除去溶液中干扰离子的一般方法是:选择试剂将干扰离子变成(7) 除去。
工业采用电解氯化钠溶液制备烧碱。某同学取电解后的溶液进行如下探究:
【提出问题】电解后的溶液中的溶质是什么?
【猜想假设】(1)NaOH、NaCl(2)NaOH
【实验探究】取电解后的溶液,进行如下实验:

【收集证据】实验1的反应现象为(1) ,实验2发生反应的化学方程式为(2) 。
【实验结论】电解后的溶液中的溶质是(3) 。
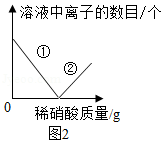
【表达交流】实验中滴加酚酞溶液的作用是(4) 。在滴加过量稀硝酸的过程中,图2中①表示的是(5) (填符号),②表示的是(6) (填符号)。
【总结规律】通过探究还可认识到:上述实验1和实验2的反应都是两种化合物在溶液中(7) 的形式,通过一种(8) 的方式而发生的复分解反应。
为了测定金属镁样品中镁的质量分数(杂质不含镁元素,不溶于水,也不与其它物质发生反应),进行了如下实验:

请回答下列问题:
(1)上述实验过程中发生反应的化学方程式为 。
(2)根据已知条件列出求解第一次所加的稀盐酸中溶质质量(x)的比例式 。
(3)此镁样品中镁的质量分数为 。
(4)用36.5%的浓盐酸配制200g上述稀盐酸,所需浓盐酸的质量为 。
(5)若将反应后的滤液蒸发104.4 g水,无晶体析出,所得溶液中溶质的质量分数为 。
(6)若要生产含镁4.5%的铝合金960 t,需要上述金属镁样品的质量为 。
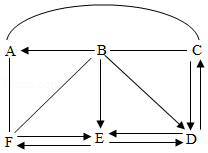
如图中A、B、C、D、E、F为初中化学常见的六种物质。F是一种黑色粉末,E是密度最小的气体,D是一种常见的液体,A与C可用于配制农药波尔多液(图中用"﹣"或  "表示两种物质能发生反应,用或"→"
"表示两种物质能发生反应,用或"→"  "表示两种物质间能单向或双向转化,部分反应物和生成物及反应条件已略去,图中部分反应需在溶液中进行,物质是溶液的只考虑溶质)。请回答下列问题:
"表示两种物质间能单向或双向转化,部分反应物和生成物及反应条件已略去,图中部分反应需在溶液中进行,物质是溶液的只考虑溶质)。请回答下列问题:
(1)分别写出A、B、E、F四种物质的化学式A 、B 、E 、F 。
(2)F与少量A溶液反应的现象是 。
(3)D转化成C的化学方程式为 。
实验室现有石灰石、氯酸钾、二氧化锰、稀硫酸、稀盐酸等药品及相关仪器和用品,请结合下列装置回答问题:

(1)①若用上述药品制取氧气,发生反应的化学方程式为 。
②仪器a的名称是 。在连接发生装置和收集装置时,将胶皮管和玻璃管连接在一起的操作是先把 ,然后稍稍用力即可把玻璃管插入胶皮管。
(2)①若用上述药品制取二氧化碳,药品的名称是 ,选择的装置是 (填字母)。
②若用澄清石灰水验证二氧化碳,实验中会观察到液面下的导管口有气泡冒出,这是因为发生装置内物质反应时气体 ,压强 ,大于外界压强,在压强差的作用下,气体从导管口冒出。
③若制取干燥的二氧化碳,需要在发生装置和收集装置之间连接 装置(填字母),该装置中的药品名称是 。
分类、类比、推理是学习化学常用的方法。
(1)随着科学研究的进展,化学实验的方法也从定性到定量发生了质的转变。若按实验方法分类,应将实验D和 (填字母)分为一类,依据是 。

(2)①观察所给粒子排列规律,将合适的化学符号填入空白:O 2 ﹣、F ﹣、 、Na +、Mg 2+。
②类比金属单质间的置换反应,某些非金属单质间也能发生置换反应,如Cl 2比Br 2活泼,能与HBr发生反应:Cl 2+2HBr═2HCl+Br 2;已知Cl 2比N 2活泼,则Cl 2与NH 3在一定条件下发生反应的化学方程式为 。