2017年5月,我国在南海海域成功开采天然气水合物﹣可燃冰,可燃冰是甲烷与水在低温、高压的条件下形成的无色、冰状固体,是最具开发前景的能源之一。可燃冰的主要成分是CH4•nH2O,在开采过程中若甲烷泄漏,会导致严重温室效应。某校化学兴趣小组的同学对甲烷燃烧的产物产生了兴趣,请你参与:
[提出问题]甲烷燃烧后生成哪些物质?
[查阅资料]含碳元素的物资完全燃烧生成CO2,不完全燃烧生成CO;无水CuSO4遇水变蓝。
[猜想与假设]
甲 CO2、H2O 乙 CO、H2O
丙 NH3、CO2、H2O 丁 CO2、CO、H2O
你认为 同学的猜想是错误的。
[实验探究]为了验证上述猜想与假设,将甲烷在一定量的纯净氧气中燃烧的产物依次通过下列装置,进行验证:
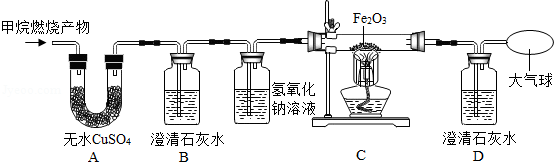
(1)A、B装置的顺序不能颠倒,原因是 。
(2)实验中用纯净O2而不用空气的原因是 。
(3)实验中观察到A中 ,B、D中澄清石灰水变浑浊,C中红色粉末变成黑色,由此推断 同学猜想成立。
(4)请写出B中澄清石灰水变浑浊的化学方程式 。
在100g的某盐酸中加入硝酸银溶液,反应为AgNO3+HCl═HNO3+AgCl↓,至恰好完全反应,经过滤、洗涤、干燥、称量得到质量为28.7g的AgCl沉淀,求盐酸的溶质质量分数。
不用火,不用电,只需拆开发热包倒入凉水,就能享用美食的自热食品,受到消费者的追捧。

[查阅资料]Ⅰ.发热包中物质的主要成分是生石灰、碳酸钠、铝粉。
Ⅱ.铝和强碱溶液反应生成氢气。
探究一:发热包的发热原理
(1)小明买了一盒自热米饭,取出发热包加入凉水,发生剧烈反应,迅速放出大量的热,写出产生该现象的主要化学反应方程式 ;同时发热包内固体物质变硬、结块。依据观察到的实验现象,小明猜想发热包内的物质可能发生多个化学反应,写出其中一个反应的化学方程式 。
(2)发热包上的安全警示图标有“禁止明火”,其原因可能是 。
(3)小明向使用后的发热包中加入稀盐酸,并对产生的气体展开进一步探究。
探究二:确定气体的成分
[猜想与假设]小明认为该气体可能是:a.H2; b. ; c.CO2和H2的混合气体。
[实验设计]小明同学设计如图实验装置,对气体成分进行探究。

[实验验证]甲装置中的实验现象是 ,丁装置中黑色的粉末逐渐变为红色,试管口有水珠产生,证明猜想c正确。若甲、乙装置交换位置, (填“能”或“不能”)确定气体中含有CO2,写出化学方程式并说明理由 。
[总结与反思]通过以上探究,小明做出如下反思:
A.发热包应密封防潮保存
B.能与水混合放出热量的物质均可做发热包的发热材料
C.使用后的发热包应包好按照垃圾分类投放
你认为其中正确的是 。
如图所示是实验室制取气体的常用装置。请回答下列问题。
(1)A装置中仪器①的名称是 ,试管口略向下倾斜的原因是 。
(2)仪器②的名称是 ,该仪器的主要作用是 。
(3)实验室用加热氯酸钾制取氧气,应选择的发生装置为 (填字母序号);若要收集较纯净的氧气,应选择的收集装置是 (填字母序号)。写出过氧化氢溶液和二氧化锰的混合物制取氧气的化学程式 。
(4)制取氧气和二氧化碳均可选择的发生装置和收集装置为 (填字母序号)。
向盛有100g稀硫酸和硫酸铜混合溶液的烧杯中滴加氢氧化钠溶液至过量,过滤、烘干并称量沉淀的质量。该反应过程如图所示。请按要求回答问题:
(1)滤液中的溶质是 (填化学式)。
(2)计算原混合溶液中硫酸铜的质量。
(3)氢氧化钠溶液的溶质质量分数。

水杨酸的化学式为C7H6O3,常用于制备阿司匹林。请根据其化学式回答下列问题:
(1)水杨酸是由 种元素组成。
(2)一个水杨酸分子中共有 个原子。
(3)水杨酸中氢元素与氧元素的质量比是 。
(4)13.8g水杨酸中含有氧元素的质量是 g。