如图所示为实验室中常见气体制备、净化、干燥、收集和进行实验探究的部分仪器(组装实验装置时,可重复选择仪器),某化学小组的同学欲利用其进行下列各化学实验。
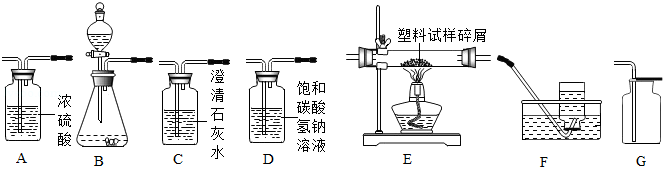
(1)用锌和稀硫酸反应制取并收集干燥的氢气,然后进行氢气的可燃性实验。
①制取氢气所发生反应的化学方程式为 。
②进行氢气的可燃性试验,点燃氢气前,一定要 。
(2)以石灰石和稀盐酸为原料,在实验室中制取并收集干燥、纯净的二氧化碳气体。按照要求设计实验装置、连接仪器,并检验装置的气密性。
①所选仪器的连接顺序为 (从左至右填写仪器序号字母)(提示:挥发出的少量HCl气体可用饱和碳酸氢钠溶液吸收)。
②二氧化碳能够扑灭木材着火的根本原因是下列的 (填写序号A、B、C、D之一)。
A.二氧化碳密度比空气大
B.二氧化碳降低了可燃物的着火点
C.二氧化碳既不能燃烧,也不支持燃烧
D.二氧化碳能与水反应
(3)以过氧化氢溶液为原料(二氧化锰作催化剂),在实验室中制取氧气,并对某种塑料试样的组成元素进行分析探究实验(资料显示该塑料只含C、H、O三种元素),所选仪器按"B→A 1→E→A 2→C碱石灰干燥管"的顺序连接,(A 1、A 2为浓硫酸洗气瓶),实验前检验装置气密性。使一定量的该塑料试样碎屑在纯氧气中充分燃烧,观察现象,收集有关实验数据(假设发生的化学反应都充分反应)。
①在该装置中,洗气瓶A 1、A 2都吸收水分,其作用的不同之处是 。
②仪器E的大玻璃管中放入的塑料试样碎屑质量为m g,塑料试样充分燃烧后,测得仪器A 2的质量增加a g,仪器C的质量增加b g,则在该塑料试样中氢、碳元素的质量之比为:氢元素的质量:碳元素的质量= (计算结果用含a、b的代数式表示)。
化学兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验(如图1),同学们观察到镁条在空气中剧烈燃烧,发出耀眼的强光,产生的大量白烟弥漫到空气中,最后在石棉网上得到一些白色固体。
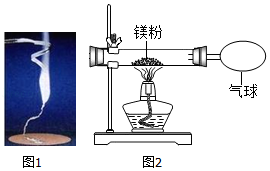
(1)请写出镁条燃烧的化学方程式 ;
(2)同学们通过称量发现:在石棉网上收集到产物的质量小于镁条的质量,有人认为这个反应不遵循质量守恒定律。你认为出现这样实验结果的原因可能是: ;
(3)小红按图2装置改进实验,验证了质量守恒定律,还发现产物中有少量黄色固体。
[提出问题]黄色固体是什么?
[查阅资料]①氧化镁为白色固体;②镁能与氮气剧烈反应产生黄色的氮化镁(Mg3N2)固体;③氮化镁可与水反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝。
[做出猜想]黄色固体是Mg3N2
[实验探究]请设计实验,验证猜想
|
实验操作 |
实验现象及结论 |
|
|
|
[反思与交流]①氮化镁中氮元素的化合价是 ;
②空气中N2的含量远大于O2的含量,可是镁条在空气中燃烧产物MgO却远多于Mg3N2,合理的解释是: 。
③同学们又联想到氢气在氯气中能够燃烧,于是对燃烧条件又有了新的认识: 。
正确选择实验仪器是实验成功的重要保证。下面是实验室中常见的仪器,请按要求填空。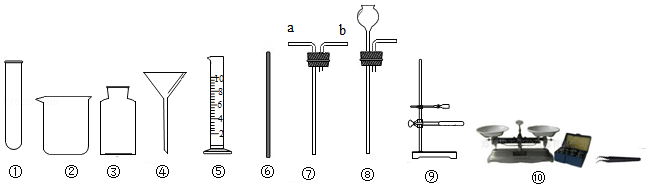
(1)配制一定溶质质量分数的氯化钠溶液,需要用到的仪器有 (填序号),还缺少的两种仪器是 (填名称);过滤粗盐水所用到的仪器有 (填序号)。
(2)实验室用锌粒和稀硫酸制取氢气,可选用上述仪器中的 (填序号)组合成发生装置。
(3)利用仪器③与⑦可组合成一个贮气装置,收集氢气(氢气难溶于水、密度小于空气)时,气体应从仪器⑦的 (填“a”或“b”)端通入,该装置还有其他的用途,请你任举一例: 。
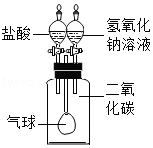
氢氧化钠溶液和二氧化碳反应没有明显现象,为验证CO 2与NaOH能够发生反应,某同学用右图组装实验装置,并进行实验。
(1)有时药品滴加顺序会影响实验现象。如果观察到的现象是"气球先膨胀,后变瘪",则加入试剂的顺序应该是 (填序号)
A.先加入盐酸,再加入氢氧化钠溶液 B.先加入氢氧化钠溶液,再加入盐酸
(2)请解释气球"先膨胀"的原因: 。
(3)写出气球"后变瘪"的化学方程式 。
控制变量法是科学探究中常用的方法之一。
(1)在探究固体物质的溶解度时,需要考虑的因素有:①溶质的种类;②溶剂的种类;③溶质最多被溶解的质量;④溶剂的质量;⑤温度。
如测定“某物质在不同温度下的溶解度”,研究的是 (填序号)受温度的影响,这就需要控制其他因素保持不变。
(2)右表是利用控制变量法测得的氯化钠、硝酸钾在不同温度时的溶解度,请根据表格内容及实验现象回答下列问题。
|
温度(℃) |
20 |
40 |
50 |
|
|
溶解度/g |
NaCl |
36.0 |
36.6 |
37.0 |
|
KNO3 |
31.6 |
63.9 |
85.5 |
|
①从上表可知,两种物质的溶解度受温度变化影响较大的是 ;
②20℃时,将等质量的NaCl、KNO3分别放入盛有100g水的两个烧杯中,充分溶解后如图1所示,升温到50℃时如图2所示。试判断:50℃时甲烧杯中的溶液一定是 (填“饱和溶液”、“不饱和溶液”或“不能确定”)。

能源、环境与人类的生活和社会发展密切相关。2017年5月18日我国宣告可燃冰试采成功,这在世界上也是首次。可燃冰外观像冰,在地球上的储量大约是已探明其他化石燃料总量的2倍;同等条件下,可燃冰燃烧产生的能力比传统的化石燃料要多出数十倍,而且燃烧后不产生任何的残渣和废气,是公认的地球上尚未开发的最大新型能源。
(1)目前,人类使用的化石燃料主要包括 。
(2)为减少污染、提高煤的利用率,可在高温条件下将其转化为可燃性气体,此过程的微观示意图如图所示,该反应的化学方程式为 。

(3)为方便贮存和运输,天然气通常被压缩到容积很小的钢瓶中,而可燃冰却很难被压缩。试从分子的角度分析,其中的原因是 。
(4)可燃冰作为新型能源,相比传统化石燃料具有很多优势,主要是 (填序号)。
A.储量丰富
B.燃烧值大
C.清洁、无污染
D.易于开采。