试用化学符号填空:
(1)氯化镁中镁元素为+2价 ;
(2)  表示的微粒是 ;
表示的微粒是 ;
(3)溶于水使溶液温度显著降低的氮肥 ;
(4)常温下为液体的金属 。
用下列化学用语填空:
稀释乳化过滤氧化蒸馏溶解吸附
(1)降低水硬度的方法 ;
(2)除去河水中泥沙的方法 ;
(3)用活性炭除去毒气 ;
(4)将溶液溶质质量分数变小 。
今年九月,我国发生“三鹿牌”奶粉受污染事件,导致食用受污染奶粉婴幼儿产生肾结石病症,其原因是奶粉中含有三聚氰胺,牛奶和奶粉中加入三聚氰胺,是因为它能冒充蛋白质,这种不法行为应该受到法律的处理.
三聚氰胺分子中碳、氮、氢的原子数之比为 ;
三聚氰胺中碳、氮、氢三种元素质量之比为 ;
三聚氰胺中氮元素的质量分数为 .
请结合下列实验常用装置,回答有关问题.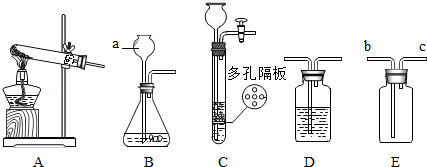
图中仪器a的名称: .
若用高锰酸钾制取氧气,应选用的发生装置是 ,在加入药品前,应首先 ,加药品后试管口还应放置一团 ,反应的化学方程式是 .
若要制取二氧化碳,在B装置中装有石灰石,那么a中应加入 ,反应的化学方程式是 . 如果用E装置收集该气体,则气体从 端进入.
实验室如用块状固体和液体无需加热制取难溶性气体,可将B装置改进为C装置,其优点是 .
学习了燃烧和灭火后,小槟设计了如图所示的实验,甲烧杯中有高低两支燃烧的蜡烛,向甲中加入适量碳酸钠和盐酸,在乙烧杯上倒扣在高低两支蜡烛上方,请你帮她分析两实验的现象有何区别: .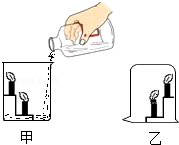
同学们注意到了吗?随着现代化建设步伐的加快,我们的生活质量正在逐步提高.请你用所学的化学知识结合生活经验回答下列事例中的有关问题;
走进厨房,你会发现煤气罐被方便、价廉的管道天然气代替了,天然气属于 能源,其主要成分在空气中充分燃烧的化学方程式为 .
走进干洗店作社会调查时,你会了解到有些干洗店用装有活性炭的新款干洗机代替旧款干洗机,可将有毒物质大约降至原来的 .这是利用了活性炭的 性.
.这是利用了活性炭的 性.
走进加油站,你会发现除了各种型号的汽油之外,还多了乙醇汽油,至2008年1月1日,包括我市在内推广使用乙醇汽油,提倡使用乙醇汽油的目的是 .