请根据下列装置图,回答有关问题:

(1)写出图中标号仪器的名称:① ;② ;
(2)写出用高锰酸钾制取氧气的化学方程式 ;
(3)用E装置收集氧气时,应等到 时开始收集;
(4)用C装置代替B装置制取二氧化碳的优点是 ;
(5)实验室常用加热无水醋酸钠与碱石灰固体混合物制取甲烷,应选择的发生装置是
(填字母);已知甲烷可用D装置收集,则甲烷的密度比空气 (填“大”或“小”)
(6)要验证二氧化碳能与水反应,F装置内应盛放 (填试剂名称);发生反应的化学方程式为 ;
(7)用F装置收集二氧化碳,验满时应将燃着的木条放在 (填“a”或“b”)端。
Mg(OH)2具有广泛的应用,常用菱镁矿制备。研究人员向一定质量的菱镁矿粉中加入过量的稀硫酸,充分溶解后除杂、过滤,得到只含MgSO4和H2SO4的混合溶液,为确定混合溶液中镁的含量,取4份混合溶液各100g,向每份混合溶液中加入一定质量的4%NaOH溶液,得到实验数据如下表所示:
|
实验编号 |
① |
② |
③ |
④ |
|
NaOH溶液质量/g |
10.0 |
20.0 |
30.0 |
40.0 |
|
Mg(OH)2质量/g |
0.232 |
0.522 |
0.580 |
0.580 |
(1)实验 (填实验编号)中硫酸镁完全反应。
(2)计算100g混合溶液中含MgSO4的质量(写出计算过程)。
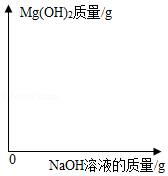
(3)分析实验数据,在图中,画出加入4% NaOH溶液质量0﹣30.0g过程中,产生Mg(OH)2沉淀质量对应的变化图,并标注必要的数值。
如图为某牙膏的部分标签,活性成分单氟磷酸钠的化学式为Na2PO3F(相对分子质量为144),请回答下列问题:
(1)人体中F属于 (填“微量”或“常量”)元素。
(2)Na2PO3F中金属元素与氧元素的质量比为 。
(3)若牙膏中其它成分不含氟,则每支这种牙膏中,含Na2PO3F的质量为 g(结果保留小数点后一位)。

某化学兴趣小组用石灰石和盐酸制取一瓶CO2,验满后,将澄清石灰水倒入集气瓶中,发现没有变浑浊。兴趣小组对这个异常现象进行了探究。
[提出问题]澄清石灰水为什么没有变浑浊?
[查阅资料](1)CO2过量时,CaCO3沉淀会转化为可溶于水的Ca(HCO3)2
(2)AgCl不溶于稀硝酸
[提出猜想]Ⅰ.石灰水已完全变质Ⅱ. Ⅲ.CO2中混有HCl
[实验方案]兴趣小组用原药品继续制取CO2,并进行探究。制备CO2的化学方程式为 。
|
步骤 |
实验操作 |
实验现象 |
结论及化学方程式 |
|
(1) |
取少量澄清石灰水于试管中,加入 溶液。 |
产生白色沉淀。 |
猜想Ⅰ不成立。 |
|
(2) |
将少量气体通入盛有澄清石灰水的试管中。 |
|
猜想Ⅱ不成立。 |
|
(3) |
将气体通入盛有 溶液的试管中,再加稀硝酸。 |
|
猜想Ⅲ成立。反应方程式为 。 |
[实验结论]制取的CO2气体中混入了HCl,所以澄清石灰水没有变浑浊。
[交流讨论]若要收集到纯净、干燥的CO2,需将混合气体依次通入饱和 NaHCO3溶液和 。
【拓展思考】回忆课本中收集呼出气体的操作后,同学们尝试用排水法收集一瓶CO2,倒入澄清石灰水后,石灰水变浑浊。你认为该实验成功的原因是 (写一点)。
某合金主要成分为Zn、Fe、Cu及这三种金属的少量氧化物。利用该合金制成的机械零件废弃物制取高纯度ZnO,其部分工艺流程如图所示。请回答:
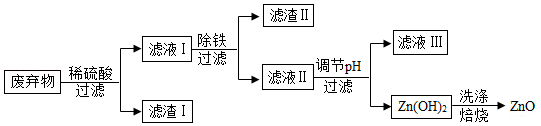
已知:Zn(OH)2溶于强碱形成可溶性盐。
(1)滤渣Ⅰ中一定有 。
(2)加酸溶解废弃物时,需要通风并远离火源,其原因是 。此过程中Zn还能起到除铜作用,除铜的化学方程式为 ,此反应属 (填基本反应类型)。
(3)调节pH可用NaOH,但不能过量,其原因是 。
(4)焙烧Zn(OH)2发生分解反应的化学方程式为 。
如图表示元素的化合价与物质类别的关系,“→”表示物质之间可以转化。A、B、C、D、E、F、G是初中化学所学物质,分别由H、O、S、Cl、K、Ba中的一种、两种或三种元素组成。请回答:
(1)A和E的化学式分别为 和 。
(2)D与G反应的化学方程式为 ,此反应属 (填基本反应类型)。
(3)A~G物质间,发生中和反应的化学方程式为 。
