硫酸亚锡(SnSO4)广泛应用于电镀工业。该物质易与氧气反应而变质。实验室模拟工业上制取SnSO4的一种实验方案如下:

(1)SnCl2由Sn与盐酸反应制得,同时生成氢气,该反应的化学方程式为 ↑ 。
(2)Na2CO3俗称 。
(3)过滤所得滤液中的溶质为 (填化学式)。
(4)用已知质量分数和密度的浓硫酸配制质量分数为15%的稀硫酸,所需玻璃仪器有烧杯、玻璃棒、胶头滴管和 。稀释浓硫酸的正确操作为 。
(5)反应2属于基本反应类型中的 反应。从反应2所得溶液中获得SnSO4晶体的部分操作须在隔绝空气条件下进行的原因是 。
铁的冶炼与利用是学习和研究化学的重要课题。
Ⅰ.铁的冶炼。竖炉炼铁的工艺流程如图1所示。
4燃烧的作用是
(2)写出“还原反应室”中炼铁的一个反应的化学方程式 。
422242的质量(m)范围是 。
323232的铜冶炼废水。在相同条件下,测量总质量相同、铁的质量分数不同的铁炭混合物对水中重金属离子的去除率,实验结果如图2所示。
2+2+2+不能被除去,其原因是 。
(2)铁炭混合物中铁的质量分数为0时,也能除去水中少量的重金属离子,其原因是 。
(3)处理效果最好时,铁炭混合物中的铁的质量分数为 。
研究小组同学对铝和稀盐酸的反应进行了探究。如图1所示实验,先检查装置气密性,再将橡皮塞连接气体压力传感器,烧瓶中放入铝片和稀盐酸,塞紧瓶塞并打开仪器,一段时间后,得到如图2所示的气体压强与时间的关系曲线图。
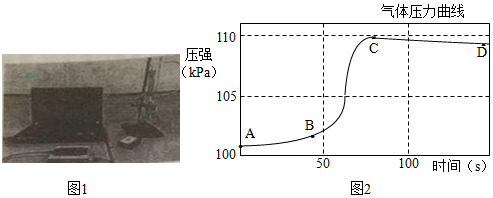
(1)铝与稀盐酸反应的化学方程式为 。
(2)AB段气体压力变化不明显的原因是 ;CD段气体压力逐渐下降的原因是 。
(3)从BC段看反应的速率是先变快后变慢,导致变慢的因素有 (填序号)
a.铝片的表面积
b.盐酸的浓度
c.温度
如图装置可用于多次连续进行氧气的制取和性质的实验。
(1)仪器Y的名称是 。
(2)水泥负载二氧化锰小球用于实验时的主要优点是 。该实验中收集氧气的方法是 。
(3)做氧气的性质实验时,实验不同,Z的作用不同。
①铁丝燃烧。Z为水,其作用是 。
②硫粉燃烧。Z为NaOH溶液,其作用是 。
③蜡烛燃烧。Z为 ,其作用是验证蜡烛中含有碳元素。
(4)实验时需要1.6g氧气,至少需要加入多少克5%的过氧化氢溶液。(写出计算过程)

某化学课外活动小组的同学为了测定某氮化镁样品中Mg3N2的质量分数,他们取氮化镁样品5.0g于烧杯中,加入100g某浓度的盐酸(足量),充分反应后(杂质不溶于水也不与盐酸反应),测得剩余固体的质量为1.0g。请计算:
(1)已知:Mg3N2与盐酸反应的生成物只有氯化镁和氯化铵,则在配平的该化学反应方程式中,HCl前面的化学计量数为 。
(2)氮化镁样品中Mg3N2的质量分数。(写出计算过程)
(3)此时所得溶液中氯化镁的质量分数。(写出计算过程)
别嘌醇片(C5H4N4O)可用于治疗因尿酸生成过多而引起的高尿酸血症;非布司他片(C16H16N2O3S)是目前治疗痛风高尿酸血症比较好的一种药物,在临床上非布司他片适用于痛风患者高尿酸血症的长期治疗。
(1)C5H4N4O的相对分子质量为 。
(2)C5H4N4O和C16H16N2O3S中,氮元素的质量分数较大的是 。