钼是一种重要的金属,用它制成的合金有良好的机械性能,在工农业生产和国防上都有广泛的用途。如图是利用钼矿石(主要成分为MoS 2)制备金属钼的流程图:
信息:MoO 3+3H 2 Mo+3H 2O
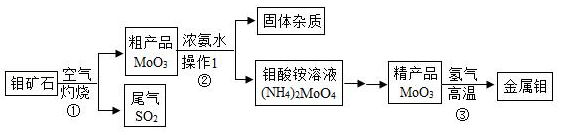
请回答下列问题:
(1)反应①常将钼矿石粉碎,目的是 ;MoO 3中钼元素的化合价为 。
(2)操作Ⅰ的名称是 ;常用NaOH溶液吸收反应①的尾气,化学方程式为 。
(3)制得19.2吨金属钼,理论上至少需含MoO 380%的粗产品多少吨?请写出计算过程。
注:粗产品杂质中不含钼元素
下列是实验室制取气体常用的部分装置。

(1)同学们为了探究影响实验室制取二氧化碳气体的因素,进行了以下四组实验:
|
药品/实验编号 |
甲 |
乙 |
丙 |
丁 |
|
大理石 |
mg,块状 |
mg,块状 |
mg,粉末状 |
mg,粉末状 |
|
盐酸(过量) |
vmL,稀盐酸 |
vmL,浓盐酸 |
vmL,稀盐酸 |
vmL,浓盐酸 |
①写出上述反应的化学方程式 ,此反应属于的基本反应类型是 ,
原来收集二氧化碳气体的装置是 (填写字母)。
②若探究盐酸的浓度对上述反应的影响,可选择实验甲与 (选填实验编号)进行对照。

(2)小丽同学选用A装置加热高锰酸钾制取氧气时发现试管固定的太高,应调节图中的旋钮 (选填“①”、“②”、“③”)。
(3)通过比较,归纳实验室制取二氧化碳和氧气的实验,总结实验室制取气体选择装置时的一般思路。
|
选择气体发生装置的依据 |
|
|
选择气体收集装置的依据 |
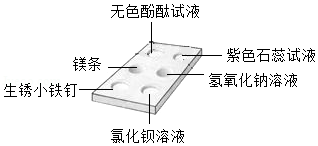
魏同学在洁净的点滴板上分别加入少量的无色酚酞试液、紫色石蕊试液、氢氧化钠溶液、氯化钡溶液、生锈小铁钉、镁条。然后向其中分别加入5~6滴稀硫酸观察现象。
(1)该实验的目的是 ,写出一个有气体产生的反应方程式 。
(2)写出稀硫酸与生锈小铁钉反应除去铁锈的化学方程式 。
金属在生活和生产中有着非常广泛的应用。金属材料已经成为社会发展的重要物质基础,研究其性质十分必要。
(1)海水中含量最多的金属元素是 (填写元素符号)。
(2)人们对金属铝的研究和利用比铜和铁晚,金属大规模开发和利用的先后顺序与金属的 有关。某同学为了验证锌、银、铜三种金属的活动性顺序。设计了五个实验:
①将锌片、铜丝分别放入稀盐酸中;②将银丝放入硝酸铜溶液中;③将铜丝放入硝酸银溶液中;④将铜丝放入硫酸锌溶液中;⑤将锌片放入硝酸银溶液中,下列实验组合能够验证锌、银、铜三种金属活动性顺序的是 (填写字母)。
A.①②B.①③C.②④D.①⑤
(3)我国古代就发明了湿法冶金技术。请你写出用铁和氯化铜为原料进行湿法炼铜的化学方程式 。
兴趣小组的同学们利用如图所示的装置探究碳的氧化物的性质(固定装置略)

(1)写出装置B中发生的化学方程式 。
(2)反应一段时间后,装置D的玻璃管中观察到的现象是 ,写出反应的化学方程式 。
(3)从保护环境的角度分析,装置F需要改进的是 。
在宏观、微观和符号之间建立联系是化学学科的特点。
(1)氢氧化钠和氢氧化钾的水溶液具有相似化学性质的原因是都含有 (用符号表示),向它们的溶液中分别滴加无色酚酞试液,观察到的现象是 。
(2)下列符号:①Hg ②N ③SO2④MgCl2⑤H2O ⑥KClO3⑦CH4中,既能表示一种元素又能表示一种原子,还能表示一种物质的是 (选填序号),能够表示氧化物的是 (选填序号)。