柠檬酸(化学式为C6H8O7)是一种果酸,有爽快的酸味,常用于固体饮料。请计算:
(1)1个柠檬酸分子中含有 个原子。
(2)柠檬酸中碳、氧元素的质量比为 (填最简整数比)。
(3)19.2g柠檬酸中含氢元素的质量为 g
工业上含铬(Cr)废水中铬的存在有+3价和+6价两种形式的化合物,其中+6价化合物的毒性最大。含铬废水一般的处理方法是将+6价的铬转化为+3价的铬,形成Cr(OH) 3沉淀而除去。
请你根据以上信息回答下列问题:
(1)含铬废水未经处理直接排放不可能造成的危害是 (填字母序号)。
A.造成水体污染 B.造成土壤污染 C.造成大气污染 D.引起人畜中毒
(2)+6价铬的化合物通常有K 2Cr 2O 7(重铬酸钾),乙醇(酒精)能将橙色K 2Cr 2O 7的硫酸溶液迅速还原成硫酸铬,其溶液中含Cr 3+而显蓝绿色,此原理可用于检查司机是否"酒驾",据此交警判断司机"酒驾"的根据是 。
(3)氢氧化钠溶液能将硫酸铬中溶液中+3价铬沉淀,其反应的化学方程式是 。
工业上炼铁炼钢和轧制钢材的主要流程如图。
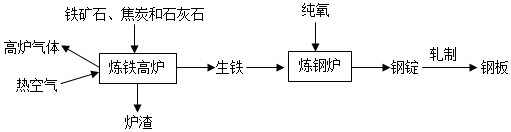
已知生铁的含量含碳量为2%﹣4.3%钢的含碳量为0.03%﹣2%。
(1)反应:①Fe 2O 3+3CO 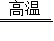 2Fe+3CO 2,②Fe 2O 3+3C
2Fe+3CO 2,②Fe 2O 3+3C  2Fe+3CO.属于置换反应的是 ,用于高炉炼铁的原理是 (填序号)
2Fe+3CO.属于置换反应的是 ,用于高炉炼铁的原理是 (填序号)
(2)炼铁的固体原料需经过粉碎,其目的是 。
(3)热空气和高炉气体的主要成分有一种相同,这种气体的化学式是 。炉渣中含有硅酸钙(CaSiO 3),其中硅元素的化合价是 。
(4)炼钢炉中,通入纯氧的目的是 。将钢锭轧成钢板,体现了金属的 性。
(5)钢铁制品可能会生锈,写出用稀硫酸除锈反应的化学方程式 。
H 2O 2分解时可以使用的触媒不止MnO 2一种。为比较相同浓度的FeCl 3溶液和CuSO 4溶液对H 2O 2分解的催化效果,某研究小组进行了如下探究(如图):
(1)写出H 2O 2分解(MnO 2作催化剂)的化学方程式 。
(2)用图甲的实验来进行定性探究,通过观察 可比较两者的催化效果是不同的。 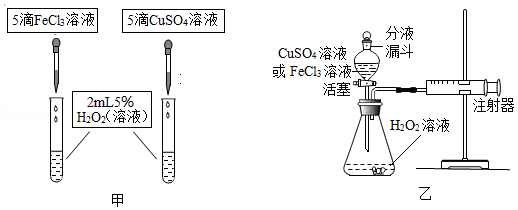
(3)用图乙的实验来进行定量探究,实验前检查该装置气密性的方法是 。要定量的比较出两者的催化效果,可测量生成等体积气体时所需的 。
(4)在FeCl 3溶液中有一种粒子起催化作用,究竟是哪一种呢?
猜想一:铁离子(Fe 3+)起催化作用; 猜想二: 起催化作用;
猜想三: 起催化作用。
请设计实验,验证猜想一:
|
实验操作 |
实验现象及结论 |
|
分别取同温度同体积同浓度的H 2O 2溶液于2支试管中,再分别加入 和 ,观察现象。 |
|
如图是实验室制取气体的部分装置,请根据你所学知识回答问题。
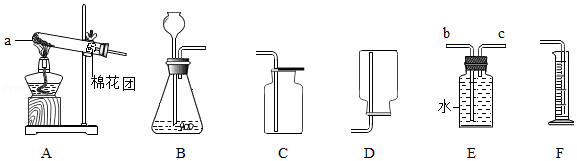
(1)玻璃仪器a的名称是 。
(2)实验室制取二氧化碳的发生装置应选取 (填字母序号),收集装置应选取 (填字母序号)。
(3)实验室只取一种固体药品用A装置来制取氧气的化学方程式是 。
(4)实验室使用B装置制取氢气时,用装置E和F组合不但能收集到比较纯净的气体,还可以测量出收集到的气体的大约体积,气体应从 (填“b”或“c”)端进入。
(5)已知化学方程式,设计实验室制取气体的发生装置,你认为应考虑的因素有 。
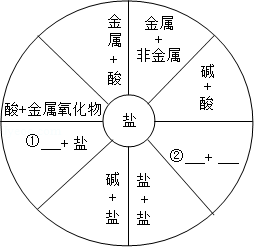
如图中各组物质(或其溶液)反应均可生成盐(中心盐)。
(1)分析图中信息,填写相应的文字,完善该图。
(2)列举相应的化学方程式说明①②:① ;② 。