根据如图所示实验回答问题。

(1)A中铜片上的白磷燃烧而热水中的白磷不燃烧,说明燃烧的条件之一是 。
(2)B中水的作用是 。
(3)C中实验现象是 。
(4)D中当观察到蒸发皿中出现 时,停止加热。
实验室固体氢氧化钠敞口放置在空气中容易变质而失效,现称取该久置于空气中的烧碱样品10.6g完全溶于蒸馏水中配成100g溶液,向其中滴加质量分数为3.7%的氢氧化钙溶液,产生沉淀与所加氢氧化钙溶液的质量关系如图所示。请通过计算回答:
(1)该烧碱样品变质的程度为 (填"部分变质"或"全部变质")。
(2)m= g。
(3)当沉淀刚好达到最大质量时,溶液中溶质质量分数为多少?(写出计算过程,计算结果精确到0.01%)

2017年6月11日,兰州国际马拉松赛如期举行。兴奋剂是国际体育界违禁药物的总称,甲基苯丙胺(C 10H 15N)是兴奋剂的一种,称之为"冰毒",该药小剂量时有短暂的兴奋抗疲劳作用。
(1)甲基苯丙胺中碳、氢、氮的质量比为 。
(2)14.9g甲基苯丙胺中氮元素的质量为 。
某校初三化学课在进行氢氧化钠化学性质教学时,同学们做了如下实验:将一定量的稀盐酸加入到盛有NaOH溶液的小烧杯中。
(1)请写出该反应的化学方程式: 。
【提出问题】实验过程中未观察到明显现象,对此同学们产生了疑问:反应后溶液中溶质是什么?
【假设猜想】针对以上疑问,第一小组同学提出如下猜想:
猜想一:只有NaCl 猜想二:有NaCl和HCl
猜想三:有NaCl和NaOH 猜想四:有NaCl、HCl和NaOH
(2)肖晓同学对以上猜想中有一种是不可能的。不可能的猜想是
【实验探究】为了验证其余猜想,各小组同学利用烧杯中的溶液,进行下列实验:
|
实验方案 |
实验操作 |
实验现象 |
实验结论 |
|
方案一 测烧杯中溶液的pH |
① |
试纸变色,与标准比色卡对比,pH<7 |
溶液中有HCl |
|
方案二 滴加CuSO 4溶液 |
取少量烧杯中的溶液于试管中,滴加几滴CuSO 4溶液 |
无明显现象 |
溶液中一定没有:② |
|
方案三 滴加Na 2CO 3溶液 |
取少量烧杯中的溶液于另一支试管中,滴加少量Na 2CO 3溶液 |
③ |
溶液中有HCl |
|
方案四 滴加AgNO 3溶液 |
再取少量烧杯中的溶液于另一支试管中,滴加少量AgNO 3溶液 |
产生白色沉淀 |
溶液中有HCl |
【得出结论】通过实验探究,全班同学一致确定猜想三是正确的。
【评价反思】老师对同学们能用多种方法进行实验探究,并且得出正确结论给予表扬,同时指出以上实验结论中有一个是错误的,请你指出错误的结论并说明原因: 。
早在春秋战国时期,我国就开始生成和使用铁器了。工业上炼铁的原理利用一氧化碳和氧化铁的反应。某校化学兴趣小组利用如图装置进行炼铁原理的实验探究(夹持装置省略)。请按要求填空:
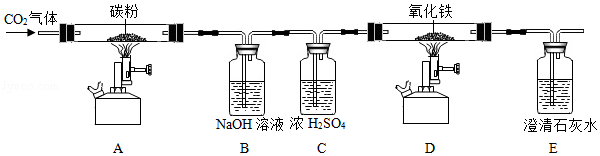
(1)写出装置A中反应的化学方程式: 。
(2)装置B的作用为 ,写出其中反应的化学方程式: ;
(3)当装置D硬质玻璃管中看到的现象为 、装置E中看到的现象为 时,说明装置D中反应发生了。
(4)同学们在讨论实验时,发现该装置存在一个不环保的缺陷,请你指出来: 。
实验室利用如图所示装置进行实验,请回答下列问题。

(1)写出图中标有字母的仪器名称:a: ;b: 。
(2)王鸿同学欲用高锰酸钾制取氧气,他选用的发生装置是 (填序号),实验时在该装置试管内靠近管口位置放一团棉花,其目的是 ;请你帮他写出反应的化学方程式: 。
(3)同学们欲用大理石和稀盐酸制取并获得干燥纯净的二氧化碳,选用装置②、④外,还选用了装置⑥两次,装置⑥中的液体依次是饱和碳酸氢钠溶液和浓硫酸,其作用分别是 、 ,气体应从装置⑥的(填"E"或"F") 端进入。