下列装置常用于实验室制取气体,请回答问题。
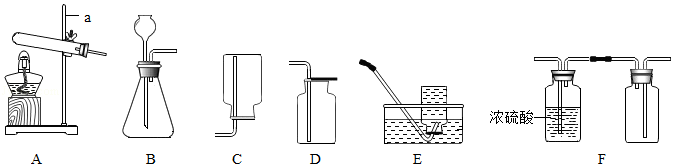
(1)仪器a的名称是 。
(2)实验室用氯酸钾和二氧化锰混合制取并收集一瓶较纯净的氧气,应选择的装置是 (填字母序号),反应的化学方程式是 。
(3)实验室可用D装置收集二氧化碳,验满的方法是 。
(4)F装置常用于干燥、收集某气体,该气体具有的性质是 。
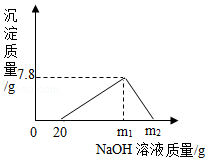
已知:Al(OH)3沉淀可溶于NaOH溶液,其反应方程式为:Al(OH)3+NaOH═NaAlO2+2H2O,现向100 g HCl和AlCl3的混合溶液中逐滴加入质量分数为20%的NaOH溶液,产生沉淀的质量与所加NaOH溶液的质量关系如图所示。回答下列问题:
(1)原混合溶液中HCl的质量分数是 。
(2)当沉淀达到最大值时生成NaCl的质量是多少?
(3)m2= 。
化学兴趣小组的同学发现实验台上有一瓶标签残缺的试剂(如图),同学们对此进行了如下探究。
【提出问题】这是一瓶什么溶液?
【猜想与假设】海天同学的猜想是Na2SO3溶液;刘浩同学的猜想是Na2SO4溶液;你的猜想是 (写一种)。
【查阅资料】
Ⅰ白色沉淀BaSO3不溶于水,但要溶于稀盐酸。
Ⅱ硝酸具有强氧化性,能将BaSO3氧化成BaSO4。
ⅢNa2SO3与稀盐酸反应产生SO2,SO2能使石灰水变浑浊,也能使品红溶液褪色。
【进行实验】
Ⅰ海天同学取适量的该溶液于试管中,滴加稀盐酸,产生无色气体,他认为自己的猜想成立,而刘浩同学认为他的结论不合理,原因是 。
Ⅱ刘浩同学为了验证自己的猜想,做了如下实验:
取适量的该溶液于试管中,先滴加足量的BaCl2溶液,再滴加过量稀硝酸,现象为 ,刘浩同学认为自己的猜想成立。
Ⅲ卓玛同学对刘浩同学的猜想又提出了质疑,她认为加BaCl2和稀硝酸,Na2SO3也会产生沉淀,为了验证自己的观点,做了如下实验:
|
步骤 |
操作 |
实验现象 |
实验结论 |
|
步骤1 |
取少量该溶液于试管中,滴加足量的BaCl2溶液 |
|
无 |
|
步骤2 |
向步骤1的试管中滴加足量的稀盐酸 |
|
此溶液不是Na2SO4 |
|
步骤3 |
将步骤2中产生的气体通入品红溶液 |
品红溶液褪色 |
|
写出卓玛同学实验过程中的化学方程式: , 。
小吴对化学实验有浓厚的兴趣,设计了如下实验装置进行实验,按要求填空.

①仪器a的名称 ;可用于实验室制取O2的发生装置有 (填装置编号,下同);实验室制取CO2的发生装置有 ;用C装置收集CO2时,气体应从C装置的 端进入(填“b”或“c”).
②实验室制取H2的化学方程式为 .
③小吴D装置的溶液中滴入石蕊试液,发现溶液显蓝色,由此可知碳酸钠溶液呈 性(填“酸”、“碱”或“中”).
④小吴用E装置探究CO2能否与碳酸钠溶液反应,他做了两组对比实验:第一组用胶头滴管向广口瓶中加入2 mL水,发现气球鼓起不明显;第二组用胶头滴管广口瓶中加入2 mL一定质量分数的碳酸钠溶液,发现气球迅速鼓起.他得出的结论是:CO2能与碳酸钠溶液反应,该反应的化学方程式为 .
初中化学几种常见物质的相互转化关系如图所示,其中A为无色无味的有毒气体,B是赤铁矿的主要成分,F常用于改良酸性土壤,H为常见的液态化合物,K是一种紫红色单质。根据推断回答下列问题:
①E溶液的颜色为 ,反应Ⅰ~Ⅲ中属于置换反应的是 (填编号),化合物Na 2DO 4中D的化合价为 。
②写出反应Ⅰ的化学方程式 ,该反应在工业上的用途是 。
③写出一个由G制取C的化学方程式 。
④D与K的混合物7 g与足量的E溶液充分反应后,固体质量增加0.8g,则该混合物中D的质量分数为 。

X、Y、Z、W是初中化学常见的四种非金属元素.X的一种原子没有中子,Y的一种单质可用于制铅笔芯,Z是地壳中含量最高的元素,W2是空气中含量最高的单质.回答下列问题:
①Y的另一种单质是天然存在的最硬的物质,该单质的名称为 ,Z2﹣的离子结构示意图为 .
②X、Z、W三种元素可形成一种盐,该盐是一种常见的化肥,其化学式为 .
③实验室检验YZ2时发生反应的化学方程式为 .
④钠与Z形成的化合物Na2Z2常用作潜水艇中的供氧剂,因为Na2Z2与YZ2反应生成Na2YZ3和Z2,写出其反应的化学方程式 .
⑤X、Y、W三种元素可按质量比2:6:7形成一种的火箭燃料偏二甲肼,其相对分子质量为60,偏二甲肼在空气中完全燃烧的产物均无污染,其化学方程式为
.