废旧电路板中主要含有塑料、铜和锡(Sn)等,为实现对锡的绿色回收,设计如下工艺流程:

已知:Sn+SnCl4═2SnCl2
(1)塑料属于 (填“有机物”或“无机物”)。
(2)SnCl2中锡元素的化合价是 。
(3)铜的金属活动性比锡的 (填“强”或“弱”);固体A中一定含有的金属元素是 。
(4)写出步骤②发生反应的化学方程式 ,其反应类型是 。
(5)相比于直接焚烧废旧电路板回收金属,该工艺的主要优点是 (回答一点)。
将氯化钠和氯化铁的固体混合物40g完全溶于101.4g水中形成溶液,再将100g一定溶质质量分数的氢氧化钠溶液分5次加入到该溶液中,充分反应后,测得的实验数据如下表所示:
|
实验次数 |
1 |
2 |
3 |
4 |
5 |
|
加入氢氧化钠溶液质量/g |
20 |
20 |
20 |
20 |
20 |
|
共生成沉淀的质量/g |
5.35 |
10.7 |
m |
21.4 |
21.4 |
求:(1)表中m的值为 。
(2)原混合物中氯化铁的质量 。
(3)恰好完全反应时,所得溶液的溶质质量分数是多少?(写出计算过程,结果精确到0.1%)
实验室有一包白色粉末,可能含有Na2SO4、Ba(NO3)2、K2CO3、KOH、CuSO4、Mg(NO3)2和KC1中的一种或几种,为了确定其成分,某化学兴趣小组进行了如下实验探究。
[查阅资料]
CaCl2溶液显中性;K2CO3和“纯碱”的化学性质极其相似;MgCO3微溶于水,不考虑为沉淀。
[实验步骤]
步骤Ⅰ:取一定量样品于烧杯中,加足量水充分溶解,有白色沉淀产生,溶液呈无色。
初步结论:原粉末中一定不含 。
步骤Ⅱ:将步骤Ⅰ中的混合物过滤,进行下一步实验探究。
[实验探究一]
小明同学对步骤Ⅱ中过滤所得滤液设计了如下的实验探究方案:
|
实验步骤 |
实验现象 |
实验结论 |
|
取一定量滤液于试管中,加入足量CaCl2溶液,充分振荡后,再滴加酚酞溶液。 |
溶液呈红色 |
由此确定原粉末中含有 |
请说明加入足量CaCl2溶液的理由 。
[猜想假设]
小红同学对步骤Ⅱ中过滤所得固体成分提出了如下猜想:
①Mg(OH)2②BaSO4③BaCO3④Mg(OH)2、BaSO4 ⑤BaSO4、BaCO3
⑥Mg(OH)2、BaCO3 ⑦Mg(OH)2、BaSO4、BaCO3
[实验探究二]
小红同学对猜想设计了如下的实验探究方案:
|
实验步骤 |
实验现象 |
实验结论 |
|
(1)取一定量过滤所得固体于试管中,加入足量稀HCl,充分振荡 |
有气泡产生,沉淀完全溶解 |
上述猜想 可能成立 |
|
(2)向(1)试管中,继续滴加足量的NaOH溶液 |
有白色沉淀产生 |
上述猜想 一定成立 |
请写出(2)中产生白色沉淀的化学方程式: 。
[归纳总结]通过上述实验验证,原粉末中仍不能确定的成分是 。
如图是实验室制取气体的常用装置: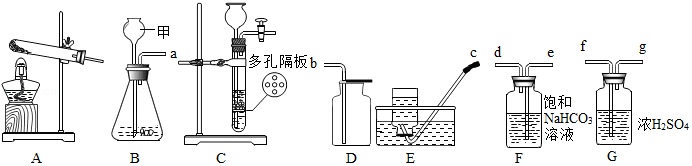
(1)仪器甲的名称是 。
(2)若选A装置作为实验室制取氧气的发生装置,反应的化学方程式为: 。实验室可用B或C装置制取二氧化碳,选用C装置相对于B装置的优点 。
(3)实验室要制取纯净干燥的二氧化碳气体,装置接口连接顺序为: a→ → → → → (填接口对应的字母,全对才得分),F装置的作用 。
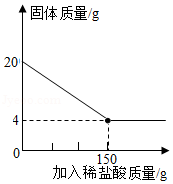
建造“南昌舰”的特种钢材需要用富铁矿石(含铁量高于50%)来冶炼。研学实践小组为测出某地赤铁矿石(主要成分是Fe2O3)中的含铁量,进行实验:取20g赤铁矿石样品,逐渐加入稀盐酸,充分反应。实验相关数据如图所示(假设杂质不溶于水,也不与酸反应)。
(1)20g赤铁矿石样品中氧化铁的质量为 g;
(2)该样品中铁元素的质量分数为 ,由此判断出该赤铁矿石 (填“属于”或“不属于”)富铁矿石。
(3)计算实验中所用稀盐酸溶质的质量分数(写出计算过程)。
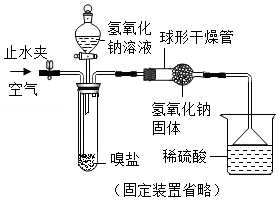
足球比赛中让意外昏迷的球员快速恢复意识会用到“嗅盐”。同学们对“嗅盐”产生了好奇,并对其成分进行如下探究。
[查阅资料]①嗅盐是由一种盐类物质和香料(不参与下列探究中的任何反应)组成,能释放出氨味气体,对人体神经会产生强烈的刺激作用,但过量吸入会危害健康。
②氯化钙稀溶液与碳酸氢铵稀溶液不发生反应。
③氨气能与硫酸化合生成硫酸铵。
[提出问题]嗅盐中盐类物质是什么?
[实验探究]填写表中空格。
|
实验 |
小军的实验 |
小英的实验 |
|
|
方案 |
嗅盐与 (填一种物质)混合研磨 |
|
|
|
现象 |
闻到较浓烈刺激性气味且试纸变蓝 |
|
|
|
结论 |
嗅盐中含有NH4+ |
嗅盐中含CO32﹣ |
确认了小军的实验结论 |
|
证明嗅盐中盐类物质是碳酸铵 |
|||
[质疑]小英认为小军的实验结论不严谨。小英通过补做一个实验(方案见上表),进而确认了小军的结论。小英的实验目的是排除嗅盐中含有 离子的可能性。
[继续探究]同学们利用如图装置进一步测定嗅盐中碳酸铵的质量分数。
反应原理:(NH4)2CO3+2NaOH X+2NH3↑+2H2O,其中X的化学式为 。
[数据记录]实验称取样品质量为m1,反应前后装有氢氧化钠固体的球形干燥管的总质量分别为m2和m3,反应前后烧杯及烧杯内溶液的总质量分别为m4和m5。
[数据处理]通过测得数据计算出嗅盐中碳酸铵的质量分数。
[反思与评价]关于该实验的说法正确的是 (填序号,双选)。
A.嗅盐中碳酸铵的质量分数表达式为: 100%
B.倒置漏斗可以增大吸收面积同时防止倒吸
C.可以用浓硫酸替代稀硫酸
D.停止加热后要通入一段时间空气,否则测定结果会偏小