某实验小组同学做中和反应实验时,向80g质量分数为10%的氢氧化钠溶液中逐滴加入稀硫酸,当恰好完全反应时,共用去稀硫酸62g。请你计算:
(1)氢氧化钠溶液中溶质的质量为 g。
(2)反应后所得溶液中溶质的质量分数?
化学与生活息息相关.
(1)2017年3月21日是第25届"世界水日",右图是我国"国家节水标志",谈谈你的理解及获得的启示: .
(2)在车水马龙的城市街道和森林茂密的公园呼吸大不一样,你能说出其中的原因吗?
.
(3)黄瓜中含有丰富的维生素C,维生素C在高温下易分解,而在酸性环境中比较稳定,为保证营养,食用黄瓜较好的方法是 .

现有生活中的两瓶无色溶液,分别是氢氧化钙溶液和稀醋酸溶液。试用三种不同的方法鉴别(不要求写出具体的操作过程和实验现象)。
(1) ;
(2) ;
(3) 。
某同学用自制电解器电解水,为了加快电解速率,可在水中加少许硫酸钠增强其导电性,当他在93.6g质量分数为5%的硫酸钠溶液中通电一段时间后,正极上产生3.2g氧气,计算:
(1)负极上产生氢气的质量;
(2)通电后溶液中硫酸钠的质量分数;
(3)该同学认为电解速率较慢,又继续向通电后的溶液中加入硫酸钠,若要使溶液中溶质的质量分数变为10%,则需要加入硫酸钠固体的质量是多少?
工业上常用电解饱和食盐水的方法制取烧碱,某化学兴趣小组为了探究久置的工业烧碱的成分,进行了如下实验:
(1)取少量样品于烧杯中,向其中加入过量稀盐酸,观察到有气泡产生,说明样品中含有 ,该反应的化学方程式为 ,接着又向烧杯中继续加入硝酸银溶液,出现了白色沉淀,甲同学立刻得出结论:样品中还含有氯化钠,乙同学对该结论提出了质疑,认为不一定含有氯化钠,理由是 ;
(2)丙同学认为除了需要确认是否含有氯化钠外,还需要确认样品中是否含有氢氧化钠,于是,大家又进行了以下实验:
①另取少量样品溶解于水,向其中加入过量硝酸钙溶液,产生白色沉淀,然后过滤、洗涤;
②向滤液中加入足量稀硝酸,再滴入硝酸银溶液后产生白色沉淀;
③向滤渣中加少量水后滴入酚酞,溶液变红.
由此判断,滤渣中的物质是 (填化学式).
(3)根据以上经验,得出的结论正确的是 (填序号)
| A. |
样品中无NaCl |
| B. |
样品中只有NaOH和Na 2CO 3 |
| C. |
样品中无NaOH |
| D. |
样品中有Na 2CO 3、NaOH和NaCl. |
工业上用海水获取粗盐以及实验室用粗盐制得精盐都包含许多化学实验知识,分析以下过程后填写下列空白:

(1)操作Ⅰ的名称是 ;
(2)海水晒盐与上述操作中 的原理相同;
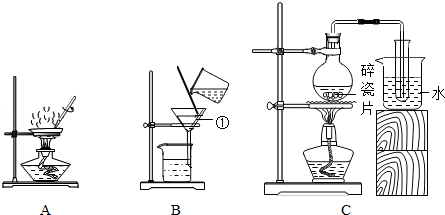
(3)上述操作可能用到下列装置,装置B中仪器①的名称是 ,用甲制取淡水可选用装置 (填序号),装置A中玻璃棒的作用是 .