对于下列实验,能正确描述其反应的离子方程式是( )
A.用Na2SO3溶液吸收少量Cl2:3SO32﹣+Cl2+H2O═2HSO3﹣+2Cl﹣+SO42﹣
B.向CaCl2溶液中通入CO2:Ca2++H2O+CO2═CaCO3↓+2H+
C.向H2O2溶液中滴加少量FeCl3:2Fe3++H2O2═O2↑+2H++2Fe2+
D.同浓度同体积NH4HSO4溶液与NaOH溶液混合:NH4++OH﹣═NH3•H2O
在相同温度下,有相同体积的甲、乙两容器,容器体积固定不变。甲容器中充入1gSO2和1gO2;乙容器中充入2g SO2和2g O2.下列叙述错误的是()
| A.化学反应速率:乙>甲 | B.平衡后SO3的浓度:乙>甲 |
| C.O2的转化率:乙>甲 | D.平衡后O2的体积分数:乙>甲 |
室温下,用某浓度NaOH溶液滴定一元酸HA的滴定曲线如图所示(横坐标为滴入NaOH的体积,纵坐标为所得混合液的pH)。下列判断正确的是()
| A.HA的浓度为1×10-4mol•L-1 | B.实验时可选甲基橙作指示剂 |
| C.pH=7时,溶液中c(Na+)>c(A-) | D.V=10mL,酸碱恰好中和 |
室温下,pH相关2的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示,下列说法正确的是()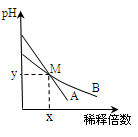
A.取等体积M点的A、B两种碱液加入同浓度的硫酸溶液至恰好完全反应时,所消耗酸溶液的体积相同
B.用醋酸中和A溶液至恰好完全反应时,溶液的pH不一定大于7
C.稀释前两溶液中H+浓度的大小关系:A=10B
D.稀释前,A溶液中由水电离出的OH-的浓度大于10-7mol/L
某化学科研小组在其他条件不变时,改变某一条件对反应[可用aA(g)+bB(g) cC(g)表示]的化学平衡的影响,得到如下图象(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率)。根据图象,下列判断正确的是()
cC(g)表示]的化学平衡的影响,得到如下图象(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率)。根据图象,下列判断正确的是()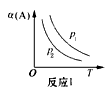
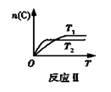
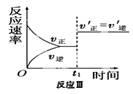
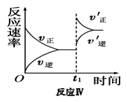
| A.反应I:若p1>p2,则此反应只能在高温下自发进行 |
| B.反应Ⅱ:此反应的△H<0,且T1<T2 |
| C.反应Ⅲ:表示t1时刻一定是使用催化剂对反应速率的影响 |
| D.反应Ⅳ:表示t1时刻增大B的浓度对反应速率的影响 |
醋酸钡晶体[(CH3COO)2Ba·H2O]是一种媒染剂,下列有关0.1mol·L-1醋酸钡溶液中粒子浓度的比较中错误的是()
| A.c(Ba2+)>c(CH3COO-)>c(OH-)>c(H+) |
| B.c(H+)=c(OH-)-c(CH3COOH) |
| C.2c(Ba2+)=c(CH3COO-)+c(CH3COOH) |
| D.c(H+)+2c(Ba2+)=c(CH3COO-)+c(OH-) |