如图是实验室气体制取、净化、干燥等常用装置图,请根据所给装置图回答问题。

(1)请写出图中标号a的仪器名称 。
(2)实验室用氯酸钾和二氧化锰混合加热制氧气,请写出该反应的化学方程式 。
(3)从A→E中选用装置完成实验室 的制取和收集,可选择的装置组合是 (填字母序号)。
(4)氨气是种无色、有刺激性气味、密度比空气小、极易溶于水的气体。实验室常用氢氧化钙固体和氯化铵固体混合加热制氨气,可以选择的发生装置是 (填字母序号)。若用I装置收集氨气,应从 (填“ ”或“ ”)端管口通入气体。
(5)若实验室无稀硫酸,改用稀盐酸和锌粒反应来制取一瓶纯净、干燥的 ,应选择的装置组合是B→ →E(填入数字序号)。
①G→H
②H→G
③F→H
④H→F
在实验室中利用下列仪器进行制取气体的实验,请回答下列问题:
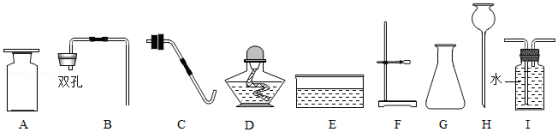
(1)写出标号仪器的名称:D ,H 。
(2)利用图中仪器可以制取二氧化碳,你选择的仪器是 (填字母,按字母顺序排列),所用药品是 。
(3)若补充一种仪器 (填仪器名称),再利用高锰酸钾以及图中仪器还可以制取氧气,其反应的化学方程式为 。
(4)若用装置I收集氧气,气体应从 端导管进入(填“左”或“右”)。
如图是初中化学的一些基本实验,请回答相关问题:

(1)A实验中集气瓶内水的作用是 。
(2)B实验中玻璃管的作用是 。
(3)C实验过程中,当蒸发皿中出现 时,停止加热。
(4)D实验中酒精灯加网罩的作用 。
掌握仪器的使用方法并严格按照操作要求进行实验,才能保障实验的成功和安全。根据所学化学知识,回答下列问题:
(1)固体药品通常保存在 里(填仪器名称)。
(2)取液后的滴管,平放或倒置可能造成的后果是 (答一点即可)。
(3)过滤液体时,玻璃棒的作用是 。
(4)用托盘天平称量12.6g氯化钠时,向左盘中加入氯化钠后,发现指针向右偏转,应进行的操作是 。
工业上以黄铁矿(主要成分是二硫化亚铁FeS2)为原料,生产硫酸。将黄铁矿(FeS2)粉碎,加入沸腾炉中瓶鼓入空气进行高温煅烧,得到气体和炉渣,气体经过一系列变化得到硫酸。请回答下列问题:
Ⅰ.FeS2中硫元素的化合价为 。
Ⅱ.将黄铁矿粉碎,目的是 。
Ⅲ.已知炉渣的主要成分为铁的某一种氧化物,甲同学对炉渣中铁的氧化物进行探究。
【查阅资料】
1.Fe3O4+8HCl═FeCl2+2FeCl3+4H2O
2.向FeCl2溶液中滴加铁氰化钾溶液,产生蓝色沉淀,而向FeCl3溶液中滴加铁氰化钾溶液不产生蓝色沉淀。
3.向FeCl3溶液中滴加无色的硫氰化钾溶液时,溶液变成红色,而向FeCl2溶液中滴加无色的硫氰化钾溶液时,溶液不变成红色。
【提出猜想】猜想1:炉渣中铁的氧化物为FeO 猜想2:炉渣中铁的氧化物为Fe2O3
猜想3:炉渣中铁的氧化物为 。(填化学式)
【方案设计】
1.取少量炉渣于烧杯中,加入过量的稀盐酸(杂质不溶于稀盐酸),充分搅拌,过滤。
2.取上述滤液少许于A、B两试管中,向A试管中滴入铁氰化钾溶液,设想有两种可能的实验现象:①产生蓝色沉淀;②不产生蓝色沉淀。向B试管中滴入少量无色的硫氰化钾溶液,设想也有两种可能的实验现象:③溶液变为红色;④溶液不变红色。
请你帮助甲同学填写猜想成立时,A、B两试管中的实验现象(用①②③④填空):
若猜想1成立,则实验现象为 。
若猜想2成立,则实验现象为 。
若猜想3成立,则实验现象为 。
【实验验证】甲同学取滤液少许于试管中,向试管中滴加铁氰化钾溶液或无色的硫氰化钾溶液中的一种试剂就证明了猜想2成立,甲同学滴加的试剂为 。
实验室进行有关碳及其氧化物的实验,装置如图(图中夹持仪器已略去)。请根据题意回答问题并填写相应的空格。

(1)实验过程如下:
①连接好装置;②检查装置气密性;③装入药品并在装置中充满二氧化碳;
④打开止水夹,缓缓通入CO2,先点燃 (填A或B)处的酒精喷灯,加热一段时间,木炭粉减少,D中有气泡产生且 ;
⑤点燃另一处酒精喷灯,一段时间后,硬质玻璃管内出现 现象时,说明CO具有 (填“氧化”或“还原”)性;
⑥关闭止水夹,熄灭两处的酒精喷灯,C中的现象为 。
(2)有同学认为该装置需要添加尾气处理装置,你认为是否需要? (填“是”或“否”),说明理由: 。
(3)写出硬质玻璃管中发生的所有反应的化学方程式 。