侯德榜是我国著名的化学家,发明了侯氏制碱法,其反应原理如下:NaCl+CO 2+NH 3+H 2O═NaHCO 3+NH 4Cl,请计算:
(1)氯化铵中氮元素的质量分数。
(2)生产8.4t碳酸氢钠,理论上需要氯化钠的质量。
合金的种类很多,用途非常广泛,黄铜是铜和锌的合金,它可以用来制造机器和电器的零件等,化学兴趣小组的同学欲测定实验室中某铜样品中铜的质量分数(不考虑黄铜中的其他杂质),请你参与他们的探究过程.
称量10g粉末状黄铜样品放入烧杯中,量取45mL稀盐酸分三次加到其中,每次充分反应后,测定生成氢气的质量,实验数据如表:
|
第一次 |
第二次 |
第三次 |
|
|
加入稀盐酸的体积(ml) |
15 |
15 |
15 |
|
生成氢气的质量(g) |
0.04 |
m |
0.02 |
试求:
(1)m的数值 .
(2)此黄铜样品中铜的质量分数是多少?(写出计算过程)
以下是实验室常用的制取气体的发生装置:

(1)写出A装置中任意两种仪器的名称 、 .
(2)若选用高锰酸钾为药品制取氧气,应选择的发生装置是 (填写字母),检验氧气的方法是 .
(3)选用3%的过氧化氢溶液和粉末状的二氧化锰混合制取一定量的氧气,你认为最理想的发生装置是 (填写字母),可采用的收集方法是 ,写出反应的化学方程式 .
化学反应过程中常常伴随产生一些现象,同学们发现将CO 2通入NaOH溶液时没有明显的现象发生,为此,他们进行了如下探究:
(1)小明把一支收集满CO 2的试管倒立在盛有饱和NaOH溶液的烧杯中(如图1所示),观察到试管内液面上升,还有另一种原因,请简要说明 .
(2)为了进一步验证CO 2与NaOH溶液确实发生了反应,小红设计了如下方案:
分别取上述实验后的溶液于A、B两支试管中(如图2所示),向试管A中滴加足量的稀盐酸,观察到的现象是 ,反应的化学方程式 ;向试管B中滴加氯化钡溶液,观察到的现象是 ,反应的化学方程式 .虽然实验的现象不同,但都能证明CO 2与NaOH溶液确实发生了化学反应.
(3)实验过程中需要吸收CO 2时,大多会选择NaOH溶液,但是,检验CO 2时常常选择新配制的澄清石灰水,请简要解释原因 .

请对如表中的化学方程式进行评价(填写评价序号),并注明化学反应类型。
|
化学方程式 |
评价 |
化学反应类型 |
|
MgCl 2 |
② |
|
|
Al+O 2 |
③ |
|
|
HCl+NaOH═NaCl+H 2O |
① |
|
|
2Fe+6HCl═2FeCl 3+3H 2↑ |
④ |
|
评价序号:① ② ③ ④ 。
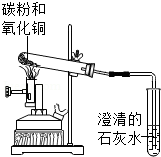
我们的祖先很早就掌握了炼铜的工艺,通过学习,同学们知道木炭可以作还原剂把氧化铜中的铜还原出来,小明查阅了大量的资料后,建议用超细炭粉与氧化铜粉末混合进行实验,他的理由是 .
(1)同学们按如图装置进行实验,当看到澄清的石灰水刚刚出现浑浊时, (填写"可以"或者"不能")确定氧化铜和炭粉已经开始反应.
(2)为了使氧化铜中的铜完全被还原,对于下列三组氧化铜和炭粉的质量比例,你建议选择 (填写字母),简要说明你的理由 .
A.36:3 B.40:3 C.48:3.