某学习小组对教材实验“在200mL烧杯中放人20 g蔗糖(C12H22O11),加入适量水,搅拌均匀,然后再加入15 mL质量分数为98%浓硫酸,迅速搅拌”进行如下探究。




 (1)观察现象:蔗糖先变黄,再逐渐变黑,体积膨胀,形成疏松多孔的海绵状黑色物质,同时闻到刺激性气味。压缩“黑色面包”时,感觉较硬,放在水中呈漂浮状态。
(1)观察现象:蔗糖先变黄,再逐渐变黑,体积膨胀,形成疏松多孔的海绵状黑色物质,同时闻到刺激性气味。压缩“黑色面包”时,感觉较硬,放在水中呈漂浮状态。 同学们由上述现象推测出下列结论:
同学们由上述现象推测出下列结论:  ①浓硫酸具有强氧化性 ②浓硫酸具有吸水性 ③蔗糖炭化得到的碳连成整体,碳原子间形成了化学键 ④浓硫酸具有酸性 ⑤黑色物质具有强吸附性
①浓硫酸具有强氧化性 ②浓硫酸具有吸水性 ③蔗糖炭化得到的碳连成整体,碳原子间形成了化学键 ④浓硫酸具有酸性 ⑤黑色物质具有强吸附性  其中依据不充分的是 (填序号);
其中依据不充分的是 (填序号);  (2)为了验证蔗糖与浓硫酸反应生成的气态产物,同学们设计了如下装置:
(2)为了验证蔗糖与浓硫酸反应生成的气态产物,同学们设计了如下装置: 
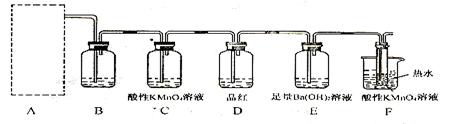
 试回答下列问题:
试回答下列问题: ①上图A中应选用下列装置 (填编号)。
①上图A中应选用下列装置 (填编号)。
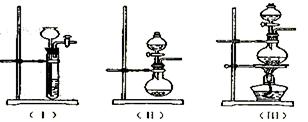
 ②B装置所装试剂是 ;D装置中试剂的作用是
②B装置所装试剂是 ;D装置中试剂的作用是  ;E装置中发生的现象是 ;
;E装置中发生的现象是 ; ③A装置中使蔗糖变黑的化学反应方程式为 ;
③A装置中使蔗糖变黑的化学反应方程式为 ; ④F装置中酸性高锰酸钾溶液颜色变浅的原因是
④F装置中酸性高锰酸钾溶液颜色变浅的原因是  ;其反应的离子方程式是 。
;其反应的离子方程式是 。
(1)已知AR2-电子数为18,则R的中子数为____________。
(2)在标准状况下,8.96L的H2X气体含有a个氢原子,则阿伏加德罗常数可表示为___________(用含a的式子表示);若其质量为13.6g ,则X的相对原子质量为___________。
(3)含13.8g Na+ 的Na3PO4溶液100mL,PO43-的物质的量浓度为___________,取出1mL,Na3PO4的物质的量浓度为_____________。
现有H 、C、O、Na四种元素,按要求完成下列各小题。
(1)写出Na+的结构示意图____________________。
(2)已知O元素的一种核素,其中子数比电子数多2,该核素可表示为:___________。
(3)A、B、C是由上述一种或几种元素组成的物质,且能实现A + B → C + H2O的转化,按要求写出化学反应方程式,并注明反应条件。
①酸性氧化物 → 盐:_________________________
②属于氧化还原反应:_________________________
(4)任写一种含上述三种元素 的非电解质________________;(填名称)上述四种元素组成的物质X可用于治疗胃酸(盐酸)过多,相应的化学方程式为_____________________________。
选择合适的装置分离提纯下列物质,将装置序号填入表格:
①②③④
| 题号 |
混合物 |
方法 |
| (1) |
海水中提取饮用水 |
__________ |
| (2) |
提取碘水中的碘 |
__________ |
| (3) |
分离MnO2和NaCl固体混合物 |
溶解、 、洗涤______ |
硝基苯甲酸乙酯在OH-存在下发生水解反应:
O2NC6H4COOC2H5+OH- O2NC6H4COO-+C2H5OH
O2NC6H4COO-+C2H5OH
两种反应物的初始浓度均为0.050 mol·L-1,15 ℃时测得O2NC6H4COOC2H5的浓度c随时间变化的数据如表所示。回答下列问题:
| t/s |
0 |
120 |
180 |
240 |
330 |
530 |
600 |
700 |
800 |
| c/mol·L-1 |
0 |
0.036 |
0.030 |
0.026 |
0.022 |
0.017 |
0.016 |
0.015 |
0.015 |
(1)计算该反应在120~180 s间的平均反应速率_________;比较120~180 s与180~240 s 区间的平均反应速率的大小,前者_________后者(填>,<或=),理由是____________________。
(2)计算15 ℃时该反应的平衡常数_____________。
(3)为提高O2NC6H4COOC2H5的平衡转化率,除可适当控制反应温度外,还可采取的措施有________。
A.加入O2NC6H4COOC2H5 B.增加OH-的浓度
C.移去产物D.加入适当的催化剂
电化学原理在化学工业中有广泛的应用.请根据如图回答问题:
(1)装置Ⅰ中的X电极的名称是 ,Y电极的电极反应式为 ,工作一段时间后,电解液的PH将 (填“增大”、“减小”、“不变”).
(2)若装置Ⅱ中a、b均为Pt电极,W为饱和食盐水(滴有几滴酚酞),实验开始后,观察到b电极周围溶液变红色,其原因是(用电极反应式表示) ,a电极上有气泡产生,该气体的电子式为 .
(3)若利用装置Ⅱ进行铜的精炼,则a电极的材料为 ,工作一段时间后装置Ⅱ电解液中c(Cu2+)将 (填“增大”、“减小”、“不变”).
(4)若装置Ⅱ中a为Ag棒,b为铜棒,W为AgNO3溶液,工作一段时间后发现铜棒增重2.1.6g,则流经电路的电子的物质的量为 .