根据下图所示实验回答下列问题:
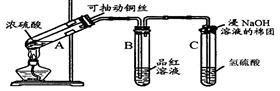
 (1)试管C口部的棉团上发生反应的离子方程式是 。
(1)试管C口部的棉团上发生反应的离子方程式是 。 (2)试管B中的实验现象是 ,若将该试管中反应后的溶液加热,可以观察到 。试管C中溶液变浑浊,则证明SO2具有 性。
(2)试管B中的实验现象是 ,若将该试管中反应后的溶液加热,可以观察到 。试管C中溶液变浑浊,则证明SO2具有 性。 (3)试管C口部的棉团既可浸碱溶液,又可浸NaHCO3溶液,其作用是 ,如果浸NaHCO3溶液,则发生反应的化学方程式是 。
(3)试管C口部的棉团既可浸碱溶液,又可浸NaHCO3溶液,其作用是 ,如果浸NaHCO3溶液,则发生反应的化学方程式是 。
已知拆开1 mol H—H键、1 mol I—I、1 mol H—I键分别需要吸收的能量为436kJ、151k J、299k J。则由氢气和碘反应生成2mol HI需要(填“放出”或“吸收”)11k J的热量。此反应中反应物的总能量(填“大于”或“小于”)生成物的总能量。物质具有的能量越(填”高”或”低”)越稳定。
根据所学知识回答下列问题,在如图所示装置中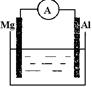 ,
,
(1)若烧杯中溶液为稀硫酸,则观察到的现象为 ,正极反应式为,负极反应式为,
该装置中的能量变化形式为。
(2)若烧杯中溶液为氢氧化钠溶液,则负极为。
A、B、C、D四种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,D的L层电子数等于K、M两个电子层上的电子数之和。
(1)C离子的结构示意图为。D在周期表中位置 。
(2)写出E的电子式:。
(3)A、D两元素形成的化合物属 (填“离子”或“共价”)化合物。
(4)写出D的最高价氧化物的水化物和A反应的化学方程式:。
(1)下列物质中:互为同素异形体的有(填序号,下同),属于同位素的有,属于同一种物质的有。
①液氯 ② Cl③白磷 ④氯气 ⑤红磷 ⑥
Cl③白磷 ④氯气 ⑤红磷 ⑥ Cl
Cl
(2)下列物质中:只存在共价键的是(填序号,下同),只存在离子键的是,既存在离子键又存在极性共价键的是,既存在离子键又存在非极性共价键的是。
①Ar ②CO2 ③Na2O2 ④KOH ⑤MgBr2⑥NH4Cl⑦CaO ⑧H2SO4
通过粮食发酵可获得某含氧有机化合物X,其相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13.0%。
(1)X的分子式是______________;
(2)X与金属钠反应放出氢气,反应的化学方程式是_____________________
(3)X与空气中的氧气在铜或银催化下反应生成Y的方程式________________;(3分)
Y能被新制的氢氧化铜氧化。其反应方程式为:______________________
(4)X与高锰酸钾酸性溶液反应可生成Z。在加热和浓硫酸作用下,X与Z反应可生成一种有香味的物质W,若184 g X和120 g Z反应能生成106 g W,计算该反应的产率。(要求写出计算过程)