有A、B、C、D四种无色溶液,它们分别是碳酸钠、硫酸钠、硫酸氢钠、氯化钡等溶液中的某一种。为确定各是何种溶液,进行了下面的实验,实验报告记录为:
①A+D 溶液+气体;
溶液+气体;
②B+C 溶液+沉淀;
溶液+沉淀;
③B+D 溶液+沉淀X;
溶液+沉淀X;
④A+B 溶液Y+沉淀;
溶液Y+沉淀;
⑤沉淀X+溶液 Y溶液+气体。
Y溶液+气体。
(1)根据以上记录,推断四种溶液中的溶质分别为(写化学式):
A:_________________,B:_________________,
C:_________________,D:_________________。
(2)写出①—⑤各反应的离子方程式。
(1)如下图所示,组成一种原电池.试回答下列问题(灯泡功率合适):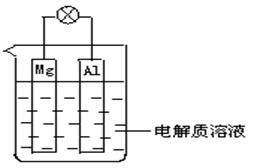
①电解质溶液为稀H2SO4时上述装置中灯泡亮,此时Al电极上发生反应的电极反应式为: ___;
②电解质溶液为NaOH溶液时,灯泡__________(填“亮”或“不亮”, 填“亮”做a题,填“不亮”做b题)。
a.若灯泡亮,则Al电极上发生反应的电极反应式为:_______________;
b.若灯泡不亮,其理由为:________________________。
(2)原电池原理的应用之一是可以设计原电池。请利用反应“Cu+2Fe3+ =2Fe2+ +Cu2+ ”设制一个原电池(正极材料用碳棒)则该电池的负极材料是,正极上发生反应的电极反应式;若导线上转移电子1.5 mol,则溶解铜的质量是。另外的重要应用是实验室在用锌与稀硫酸反应制备氢气时,可向溶液中滴加少量硫酸铜溶液,其作用是:。
将锌片和铜片以下图所示两种方式分别插入同浓度稀硫酸中。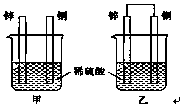
(1)以下叙述中,正确的是(填标号)。
| A.装置甲、乙中铜片表面均无气泡产生 |
| B.装置甲、乙中稀硫酸的浓度均减小 |
| C.装置乙中锌片是正极,铜片是负极 |
| D.装置乙中产生气泡的速率比装置甲快 |
(2)装置乙中,总反应的离子方程式为 ;若导线上通过0.2 mol电子,消耗锌的质量为 g。
下表是元素周期表的一部分,根据表中10种元素,用元素符号或化学式填空。
| 主族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0族 |
| 2 |
① |
② |
||||||
| 3 |
③ |
④ |
⑤ |
⑥ |
⑦ |
|||
| 4 |
⑨ |
⑧ |
⑩ |
(1)①~⑩元素中,金属性最强的是;化学性质最不活泼的是。
(2)①~⑩元素中,最高价氧化物水化物呈两性的是,该化合物与NaOH溶液反应的离子方程式为;
(3)①~⑩元素中,最高价氧化物水化物酸性最强的是,碱性最强的是;
(4)⑤、⑥、⑧、⑨所形成的离子,其半径由小到大的顺序是。
下列物质中:
(1)互为同分异构体的有(2)互为同素异形体的有
(3)属于同位素的有(4)属于同一种物质的有。(填序号)
①氯;②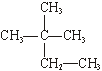 ;③白磷;④氯气;
;③白磷;④氯气;
⑤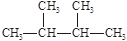 ;⑥
;⑥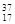 Cl;⑦
Cl;⑦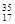 Cl;⑧红磷
Cl;⑧红磷
下列是三个不同短周期部分元素的原子半径及主要化合价:
| 元素代号 |
W |
R |
X |
Y |
Z |
| 原子半径/nm |
0.037 |
0.154 |
0.066 |
0.070 |
0.077 |
| 主要化合价 |
+1 |
+1 |
-2 |
-3、+5 |
+2、+4 |
试回答下列问题:
(1)五种元素中原子半径最大的元素是(填元素符号),画出该元素的原子结构示意图:。
(2)W、X和Y可组成一化合物,其原子个数比为4:3:2,则该化合物属(填“离子化合物”或“共价化合物”),存在的化学键是。写出该化合物与由W、R和X按原子个数比为1:1:1组成化合物反应的化学方程式:
。
(3)写出下列反应的化学方程式:
Z的单质与Y元素的最高价氧化物对应的水化物反应:。