下面是苯和一组稠环芳香烃的结构式: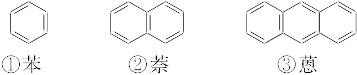

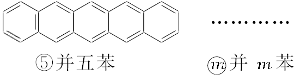
(1)写出化合物②—⑤的分子式:
①C6H6,②_________,③_________,④_________,⑤_________。
(2)这组化合物的分子式通式是C________H________(请以含m的表示式填在横线上,m=1,2,3,4,5…)。
(3)由于取代基的位置不同产生的异构现象,称为官能团位置异构。一氯并五苯有_________(填数字)个异构体;二氯蒽有_________(填数字)个异构体。
火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当把0.4mol液态肼和0.8mol H2O2混合反应,生成氮气和水蒸气,放出256.7kJ的热量(相当于25℃、101 kPa下测得的热量)。
(1)反应的热化学方程式为。
(2)又已知H2O(l)=H2O(g) ΔH=+44kJ/mol。则16g液态肼与液态双氧水反应生成液态水时放出的热量是kJ。
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是 。
。
根据下图所示,推断物质X的化学式。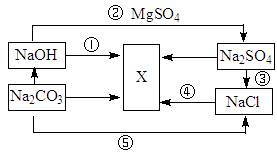
X的化学式
某混合物由NaCl、MgCl2两种物质组成,其中Na和Mg两种元素的质量比为23∶12。求
⑴NaCl与MgCl2的物质的量之比。
⑵氯离子总量为8mol时,Mg2+的物质的量是 。
。
8.4g N2与9.6g某单质Rx,所含原子个数相同,且分子数之比为3:2,则R的相对原子质量是,x值为。
同温同压下,某瓶充满氧气时质量为116g,充满二氧化碳时,质量为122g,充满气体A时质量为114g,A的摩尔质量为________。