相对分子质量为92的某芳香烃X是一种重要的有机化工原料,研究部门以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去)。其中A是一氯代物,H是一种功能高分子,链节组成为C7H5NO。
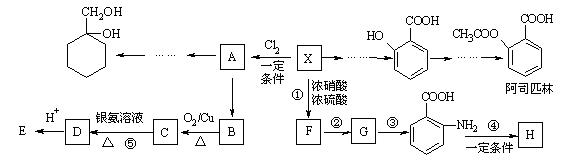
已知:
Ⅰ 
Ⅱ 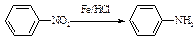 (苯胺,易被氧化)
(苯胺,易被氧化)
请根据所学知识与本题所给信息回答下列问题:
⑴H的结构简式是______________;
⑵反应②的类型是 ;
⑶反应⑤的化学方程式是____________________________________________;
⑷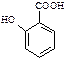 有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有________种;
有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有________种;
⑸请用合成反应流程图表示出由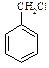 和其他无机物合成
和其他无机物合成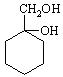 最合理的方案(不超过4步),请在答题纸的方框中表示。
最合理的方案(不超过4步),请在答题纸的方框中表示。
 例:
例: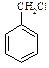

某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示。
(1)由图中的数据分析,该反应的化学方程式为;
(2)反应开始至5min Z的平均反应 速率为, X的转化率为;
速率为, X的转化率为;
(3)5min后Z的生成速率比5min末Z的生成速率(大、小、相等)。
A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。
(1)A中反应的离子方程式为____________________。
(2)B中Sn极的电极反应式为____________________,
Sn极附近溶液的pH___________(填“增大”、“减小”或“不变”)。
(3)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是____ ____________________。
____________________。
(1)下列反应中,属于放热反应的是,属于吸热反应的是。
①燃烧反应②炸药爆炸③酸碱中和反应④二氧化碳通过炽热的碳
⑤食物因氧化而腐败⑥Ba(OH)2·8H2O与NH4Cl反应⑦铁粉与稀盐酸反应
(2)写出(1)中⑥的化学方程式。
利用核磁共振技术测定有机物分子的三维结构的研究获得了2002年诺贝尔化学奖。在有机物分子中,不同氢原子的核磁共振谱中给出的峰值(信号)也不同, 根据峰值(信号)可以确定有机物分子中氢原子的种类和数目。
根据峰值(信号)可以确定有机物分子中氢原子的种类和数目。
(1)下列物质中,其核磁共振氢谱中给出的峰值(信号)只有一个的是。
| A.CH3CH3 | B.CH3COOH | C.CH3COOCH3 | D.CH3OCH3 |
(2)化合物A和B的分子 式都是C2H4Br2, A的核磁共振氢谱图如下图所示,则A的结构简式为:,请预测B的核磁共振氢谱上有个峰(信号)。
式都是C2H4Br2, A的核磁共振氢谱图如下图所示,则A的结构简式为:,请预测B的核磁共振氢谱上有个峰(信号)。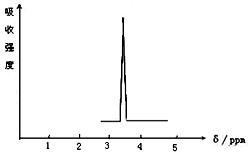
(3)化合物C的分子式是C10H14,核磁共振氢谱图如 下图所示,则C的结构简式为:。
下图所示,则C的结构简式为:。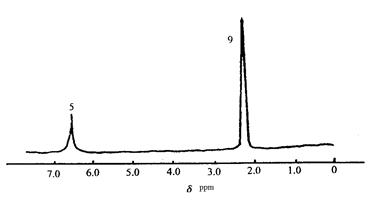
某烃A的相对分子质量是156,在CCl4溶液中跟Br2不起反应,但在光照下,Br2可以跟A起取代反应,取代产物的相对分子质量是235的有两种:产量较多的一种是B,产量较少的一种是C。另外,还可得到相对分子质量为314的产物多种。
(1)请写出A、B、C的结构简式:
ABC
(2)相 对分子质量为314的产物有种。
对分子质量为314的产物有种。