(本题共9分)化学能在一定的条件下可以转化为电能。
(一)现有如下两个反应:
① 2FeCl3 + Cu = 2FeCl2 + CuCl2
②Na2CO3 + 2HCl =" 2NaCl" + H2O + CO2↑
(1)根据两个反应的本质判断,您认为可以设计成原电池的是 (填反应序号),理由是 。
(二)请根据Zn + CuSO4 = ZnSO4 + Cu反应,选择适宜的材料和试剂设计一个原电池。
(2)画出原电池装置图,并在图中标注出电极和电解质溶液的名称。
(3)写出该原电池电极反应式:正极: ;负极: 。
下图中A、B、C、D、E、F、G均为有机化合物。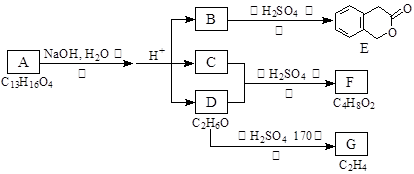
根据上图回答问题:
(1)D的化学名称是。
(2)反应③的化学方程式是 。(有机物须用结构简式表示)
(3)B的分子式是。A的结构简式是。反应①的反应类型是。
(4)符合下列3个条件的B的同分异构体的数目有个。
①含有邻二取代苯环结构、②与B有相同官能团、③不与FeCl3溶液发生显色反应。
写出其中任意一个同分异构体的结构简式。
(5)G是重要的工业原料,用化学方程式表示G的一种重要的工业用途。
(1)某一反应体系中有反应物和生成物共5种物质:S、H2S 、HNO3、NO 、H2O;则该反应中还原产物是_____;若反应过程中转移了0.3mol电子,则氧化产物的质量是_____g。
(2)将a mol Cl2通入含b mol FeBr2的溶液中,当0< a / b≤1/2 时,反应的离子方程式为:
2Fe2+ + Cl2 = 2Fe3+ + 2Cl-,写出另2个可能发生的离子方程式。
①当 a / b =1时;
②当a / b≥3/2时。
(3)观察如下反应,总结规律,然后完成下列问题:
①Al(OH)3+H2O  Al(OH)4-+ H+ ;② Cl2+2OH-= Cl-+ ClO-+H2O
Al(OH)4-+ H+ ;② Cl2+2OH-= Cl-+ ClO-+H2O
(Ⅰ)已知B(OH)3是一元弱酸,试写出其电离方程式:;
(Ⅱ)单质氰(CN)2是类卤素,试写出其与氢氧化钠溶液反应的离子方程式。
醇与氢卤酸反应是制备卤代烃的重要方法。实验室制备溴乙烷和1-溴丁烷的反应如下: ① NaBr+H2SO4 = HBr+NaHSO4;②R-OH+HBr R-Br+H2O
R-Br+H2O
可能存在的副反应有:醇在浓硫酸的存在下脱水生成烯和醚,Br-被浓硫酸氧化为Br2等。有关数据列表如下
| 乙醇 |
溴乙烷 |
正丁醇 |
1-溴丁烷 |
|
| 密度/g·cm-3 |
0.7893 |
1.4604 |
0.8098 |
1.2758 |
| 沸点/℃ |
78.5 |
38.4 |
117.2 |
101.6 |
请回答下列问题:
(1)溴代烃的水溶性 (填“大于”、“等于”或“小于”)相应的醇;其原因是。
(2)将1-溴丁烷粗产品置于分液漏斗中加水,振荡后静置,产物在(填“上层”、“下层”或“不分层”)。
(3)制备操作中,加入的浓硫酸必须进行稀释,目的是 。(填字母)
a.减少副产物烯和醚的生成 b.减少Br2的生成
c.减少HBr的挥发 d.水是反应的催化剂
(4)欲除去溴代烷中的少量杂质Br2,下列物质中最适合的是。(填字母)
a.NaI b.NaOH c.NaHSO3 d.KCl
(5)在制备溴乙烷时,采用边反应边蒸出产物的方法,其有利于;但在制备1-溴丁烷时却不能边反应边蒸出产物,其原因是。
U、V、W、X、Y、Z是原子序数依次增大的六种常见元素。Y的单质在W2中燃烧的产物可使品红溶液褪色。Z和W元素形成的化合物Z3W4具有磁性。U的单质在W2中燃烧可生成UW和UW2两种气体。X的单质是一种金属,该金属在UW2中剧烈燃烧生成黑、白两种固体。
请回答下列问题:
(1)V的单质分子的结构式为 ,XW的电子式为 ;
(2)Z元素在周期表中的位置是。
(3)元素U、V、W形成的10电子氢化物中,沸点较低的是(写化学式);结合H+能力较强的是(写化学式);用一个离子方程式加以说明。
(4)YW2气体通入BaCl2和HNO3的混合溶液,生成白色沉淀和无色气体VW,有关反应的离子方程式为,由此可知VW和YW2还原性较强的是(写化学式)。
A是生产某新型工程塑料的基础原料之一,分子式为C10H10O2,其分子结构模型如图,所示(图中球与球之间连线代表化学键单键或双键)。
(1)根据分子结构模型写出A的结构简式 ___________;
(2)拟从芳香烃 出发来合成A,其合成路线如下:
出发来合成A,其合成路线如下:
已知:A在酸性条件下水解生成有机物B和甲醇。
(a)写出⑤反应类型__________;写出H的结构简式 ___________
(b)已知F分子中含有“—CH2OH”,通过F不能有效、顺利地获得B,其原因是 _______
(c)写出反应方程式(注明必要的条件)
⑥ ________________________________________________________
⑦ __________________________________________________________
(3)A的同分异构体有多种,同时满足下列条件A的同分异构体有种:
ⅰ.含有苯环,苯环上有两个侧链且苯环上一氯取代物有两种;
ⅱ.与A有相同的官能团。