下表是元素周期表的一部分,回答下列问题: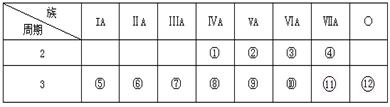
(1)写出①-——⑿号元素的元素符号① ② ③ ④
⑤ ⑥ ⑦ ⑧ ⑨ ⑩ ⑾ ⑿
(2)写出①、③两种元素形成的化合物有两种,化学式: , 。
(3)写出①元素最高价氧化物的电子式和结构式 , 。
(4)这些元素的最高价氧化物的对应水化物中________酸性最强;________碱性最强;能形成两性氢氧化物的元素是________ ,形成两性氢氧化物化学式 。
下列为合成聚合物F的路线图:

请根据以上信息,回答下列问题:
(1)A中含有官能团的名称是_________ ,C的系统命名是 。
(2)B+D→E的反应类型是_______。
(3)C生成D的反应化学方程式为__________,如果C与NaOH的醇溶液反应,则反应类型为__________。
(4)G物质的相对分子质量比 的相对分子质量大2,则符合下列条件的G的同分异构体有_ __种。
的相对分子质量大2,则符合下列条件的G的同分异构体有_ __种。
①分子中含有苯环,且苯环上有两个取代基
②遇氯化铁溶液变紫色
(1)中学常见的某有色物质,全部由短周期元素组成,能与水发生氧化还原反应,但反应中水既不作氧化剂也不作还原剂。试写出符合条件的两种物质(写化学式)________、________。
(2)在一定条件下,RO3n-和I-发生反应,离子方程式为: RO3n-+6I-+6H+=R-+3I2+3H2O , RO3n-中R元素的化合价为 ,R元素的原子最外层电子有 个。
利用I2的氧化性可测定钢铁中硫的含量。做法是将钢铁中的硫转化为H2SO3,然后用一定浓度的I2溶液进行滴定,所用指示剂为 ,该滴定反应的离子方程式为 。
右图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此回答:
(1)该试剂的物质的量浓度为 mol·L-1
用该硫酸配制100 mL 4.6 mol·L-1的稀硫酸需用量筒量取该硫酸 mL。量取浓硫酸时应选用 (选填序号:①10mL、②50mL 、③100mL)规格的量筒;可供选用的仪器有:①胶头滴管②烧瓶 ③烧杯 ④ 药匙 ⑤量筒 ⑥托盘天平。
配制稀硫酸时,上述仪器中还缺少的仪器有 (写仪器名称);
(2)将铜片与该浓硫酸加热反应所产生的气体通入新制氯水中,发生反应的离子方程式是 ;
“张-烯炔环异构反应”被《Name Reactions》收录。该反应可高效构筑五元环化合物:
(R、R‘、R“表示氢、烷基或芳基)
合成五元环有机化合物J的路线如下:
已知: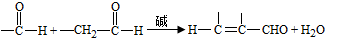
(1)A属于炔烃,其结构简式是 。
(2)B由碳、氢、氧三种元素组成,相对分子质量是30。B的结构简式是 。
(3)C、D含有与B相同的官能团,C是芳香族化合物,E中含有的官能团是 。
(4)F与试剂a反应生成G的化学方程式是 ;试剂b是 。
(5)M和N均为不饱和醇。M的结构简式是 。
(6)N为顺式结构,写出N和H生成I(顺式结构)的化学方程式: 。
废旧印刷电路板是一种电子废弃物,其中铜的含量达到矿石中的几十倍。湿法技术是将粉碎的印刷电路板经溶解、萃取、电解等操作得到纯铜等产品。某化学小组模拟该方法回收铜和制取胆矾,流程简图如下: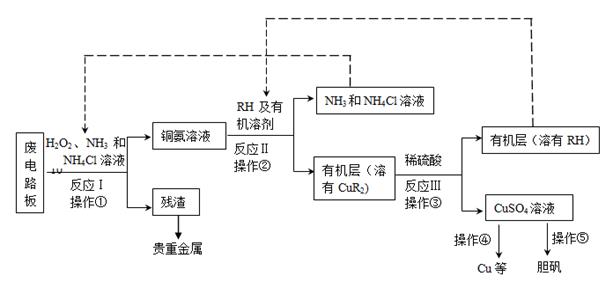
回答下列问题:
(1)反应Ⅰ是将Cu转化为Cu(NH3)42+,反应中H2O2 的作用是 。写出操作①的名称: 。
(2)反应II是铜氨溶液中的Cu(NH3)42+与有机物RH反应,写出该反应的离子方程式: 。操作②用到的主要仪器名称为 ,其目的是(填序号) 。
a.富集铜元素
b.使铜元素与水溶液中的物质分离
c.增加Cu2+在水中的溶解度
(3)反应Ⅲ是有机溶液中的CuR2与稀硫酸反应生成CuSO4和 。若操作③使用下图装置,图中存在的错误是 。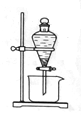
(4)操作④以石墨作电极电解CuSO4 溶液。阴极析出铜,阳极产物是 。操作 ⑤由硫酸铜溶液制胆矾的主要步骤是 。
(5)流程中有三次实现了试剂的循环使用,已用虚线标出两处,第三处的试剂是 。循环使用的NH4Cl在反应Ⅰ中的主要作用是 。