(1)完成下列基本计算:
①3.6 g H2O的物质的量为 mol;
②分子数为3.01×1023的H2的物质的量为 mol;
③标准状况下,8.96 L N2的物质的量为 mol;
④75 mL 2.0 mol·L-1 CaCl2溶液中含CaCl2 mol。
(2)选出下列各小题物质分离或提纯所依据的物理性质和分离方法。
| |
性质差异 |
分离方法 |
| ①除去氯化钠溶液中的泥沙 |
|
|
| ②用四氯化碳提取溴水中的溴单质 |
|
|
| ③分离乙酸(沸点1180C)与乙酸乙酯(沸点77.10C) |
|
|
| ④分离汽油和水 |
|
|
| ⑤从含有少量NaCl的KNO3溶液中提取KNO3 |
|
|
性质差异:A、溶解度随温度变化差异 B、在不同溶剂中的溶解度差异
C、沸点差异 D、互不相溶 E、在水中的溶解度差异
分离方法:a、蒸馏 b、过滤 c、分液 d、萃取 e、结晶
(3)工业电解食盐水制取氯气的化学方程式: 。
(本题共12分,2分/空)有下列八种不饱和烃: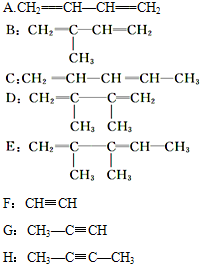
(1)已知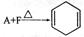 ,若要合成
,若要合成 ,则下列所选原料正确的是__。
,则下列所选原料正确的是__。
①D和H ②E和H ③E和F ④B和H ⑤C和H ⑥D和G
(2)B和Br2的CCl4溶液发生反应时,可生成多种产物,写出这些产物的结构简式,,,。
今有室温下四种溶液,有关叙述不正确的是( )
| ① |
② |
③ |
④ |
|
| 浓度c/mol/L |
0.1 |
0.1 |
0.1 |
0.1 |
| 溶液 |
氨水 |
CH3COONa溶液 |
醋酸 |
盐酸 |
A.在20 mL ①溶液中逐滴加入③溶液,溶液导电能力变化如下图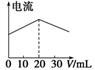
B.②、③两溶液等体积混合,离子浓度:2c(Na+)=c(CH3COO-)+c(CH3COOH)
C.①、④两溶液等体积混合,离子浓度:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
D.用④滴定①,滴定曲线如下图,可用酚酞作指示剂
11分)铁及其化合物在日常生活、生产中应用广泛.研究铁及其化合物的应用意义重大.
I.水体的净化和污水的处理与铁及其化合物密切相关.
(1)自来水厂常用高铁酸钠(Na2FeO4)改善水质.简述高铁酸钠用于杀菌消毒同时又起到净水作用的原理 .
(2)碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂,在医药上也可用于治疗消化性溃疡出血.工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如下: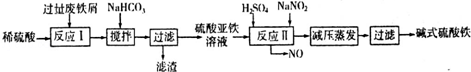
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 |
Fe(OH)3 |
Fe(OH)2 |
Al(OH)3 |
| 开始沉淀 |
2.3 |
7.5 |
3.4 |
| 完全沉淀 |
3.2 |
9.7 |
4.4 |
回答下列问题:
①写出反应I中主要发生的氧化还原反应的离子方程式 .
②加入少量NaHCO3的目的是调节溶液pH,应控制pH的范围为 .
③在实际生产中,反应II常同时通入O2以减少NaNO2的用量,若通入5.6L O2(标准状况),则相当于节约NaNO2的质量为 g.
④碱式硫酸铁溶于水后产生的[Fe(OH)]2+离子,可部分水解生成[Fe2(OH)4]2+聚合离子.该水解反应的离子方程式为 .
II铁的化合物也是制备高能锂电池的重要原料.已知磷酸亚铁锂电池总反应为:FePO4+Li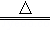 LiFePO4,电池中的固体电解质可传导Li+.试写出该电池充电时的阳极反应式 .
LiFePO4,电池中的固体电解质可传导Li+.试写出该电池充电时的阳极反应式 .
(1)环境专家认为可以用铝将水中的NO3﹣ 转化为N2,从而清除污染.该反应中涉及的粒子有:H2O、Al、OH﹣、Al(OH)3、NO3﹣、N2,请将各粒子分别填入以下空格(请将整个方程式配平后写在答题纸上).
NO3﹣+ + → + + ﹣ 该反应过程中,被氧化与被还原的元素的物质的量之比为 .
(2)若4Al(s)+3O2(g)=2Al2O3(s)△H=﹣a KJ/mol
Fe2O3(s)+C(s)=CO2(g)+2Fe (s)△H="+b" KJ/mol
C(s)+O2(g)=CO2(g)△H=﹣c KJ/mol
写出Al与氧化铁发生铝热反应的热化学方程式: .
(3)将一定质量的钠铝合金置于水中,合金全部溶解,得到20mL PH=14的溶液,然后用2mol/L的盐酸滴定,可得到沉淀量与消耗的盐酸体积关系如图:则反应过程中产生氢气的总体积为 L(标准状况)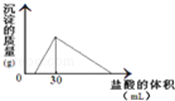
有A、B、C、D四种含硅元素的物质,它们能发生如下反应:
①C与烧碱反应生成A和水;②A溶液与钙盐溶液反应生成白色沉淀D;
③B在空气中燃烧生成C;④C在高温下与碳反应生成单质B.
根据上述变化,完成下列问题:
(1)写出B、D的化学式:B 、D .
(2)写出C与烧碱反应的化学方程式: .写出A溶液与钙盐溶液反应的离子方程式: .