常温下,金属钠和氧气反应的产物(氧化钠)中总会混杂少量的过氧化钠。因此,生产中用金属钠制备氧化钠,采用以下反应:2NaNO2+6Na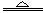 4Na2O +N2 。
4Na2O +N2 。 ⑴上述反应的氧化剂是 ,氧化产物是 ;
⑴上述反应的氧化剂是 ,氧化产物是 ;
 ⑵采用上述方法的主要原因是 。
⑵采用上述方法的主要原因是 。
光刻胶是一种应用广泛的光敏材料,其合成路线如下(部分试剂和产物略去):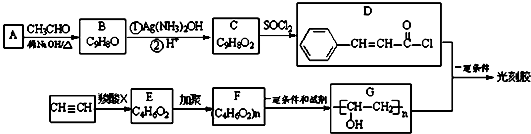
已知:A是苯甲醛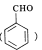
Ⅰ.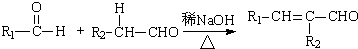 (R,R′为烃基或氢)
(R,R′为烃基或氢)
Ⅱ. (R,R′为烃基)
(R,R′为烃基)
(1)C分子中所含官能团名称为。
(2)乙炔和羧酸X加成生成E,E的核磁共振氢谱为三组峰,且峰面积比为3:2:1,E能发生水解反应,则E的结构简式为。
(3)由C到D的反应类型为。
(4)D和G反应生成光刻胶的化学方程式为。
(5)C的一种同分异构体满足下列条件:
①能发生银镜反应,其水解产物之一能与FeCl3溶液发生显色反应;
②苯环上的一氯取代产物只有两种。
写出该同分异构体的结构简式:。
(6)根据已有知识并结合相关信息,写出以CH3CHO为原料制备CH3COCOCOOH的合成路线流程图(无机试剂任用)。合成路线流程图示例如下: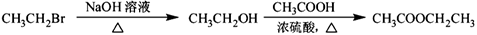
工业上用闪锌矿(主要成分为ZnS,还含有CdS、Fe2O3等杂质)为原料生产ZnSO4·7H2O的工艺流程如下:(已知Cd的金属活动性介于Zn和Fe之间)
(1)从滤渣A中可获得一种淡黄色非金属单质的副产品,其化学式为。
(2)浸取时Fe2(SO4)3与ZnS发生反应的化学方程式为。
(3)除铁过程控制溶液的pH在5.4左右,该反应的离子方程式为。
该过程在空气入口处设计了一个类似淋浴喷头的装置,其目的是。
(4)置换法除去重金属离子Cd2+,所用物质C为。
(5)取28.70 g ZnSO4·7H2O加热至不同温度,剩余固体的质量变化如图所示。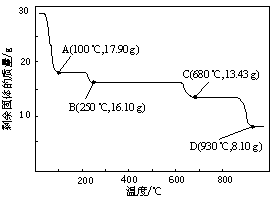
680℃时所得固体的化学式为。
a.ZnO b.Zn3O(SO4)2c.ZnSO4 d.ZnSO4·H2O
(12分)A、B、C、D、E、F为原子序数依次增大的短周期主族元素。A、F原子的最外层电子数均等于其周期序数,F原子的电子层数是A的3倍;B原子核外电子分处3个不同能级且每个能级上的电子数相同;A与C形成的分子为三角锥形;D原子p轨道上成对电子数等于未成对电子数;E原子核外每个原子轨道上的电子都已成对,E电负性小于F。
(1)写出B的基态原子的核外电子排布式:。
(2)A、C形成的分子极易溶于水,其主要原因是。与该分子互为等电子体的阳离子为。
(3)比较E、F的第一电离能:EF。(选填“>”或“<”)
(4)BD2在高温高压下所形成的晶胞如图所示 。该晶体的类型属于(选填“分子”、“原子”、“离子”或“金属”)晶体,该晶体中B原子的杂化形式为。
。该晶体的类型属于(选填“分子”、“原子”、“离子”或“金属”)晶体,该晶体中B原子的杂化形式为。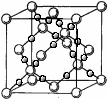
(5)光谱证实单质F与强碱性溶液反应有[F(OH)4]-生成,则[F(OH)4]-中存在。(填序号)
a.共价键
b.非极性键
c.配位键
d.σ键
e.π键
(12分)高氯酸钾广泛用于火箭及热电池业。实验室制取高氯酸钾的步骤为:称取一定质量的KCl、NaClO4溶解,然后混合,经冷却、过滤、滤出晶体用蒸馏水多次洗涤及真空干燥得到。
有关物质溶解度与温度的关系如下表: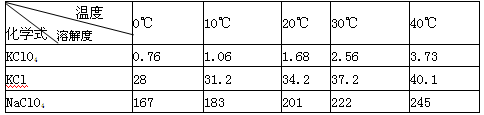
(1)写出实验室制取高氯酸钾的化学方程式:;用蒸馏水多次洗涤晶体的目的是:。
(2)Fe和KClO4反应放出的热量能为熔融盐电池提供550-660℃的温度,使低熔点盐熔化导电,从而激活电池,这类电池称为热电池。Li/FeS2热电池工作时,Li转变为硫化锂,FeS2转变为铁,该电池工作时,电池总反应为:。
(3)Fe和KClO4作为热电池加热材料的供热原理为:KClO4 (s)+4Fe(s)=" KCl" (s)+ 4FeO(s),△H< 0。
①600℃时FeO可部分分解生成Fe3O4,写成有关的化学方程式:。
②称取一定质量上述加热材料反应后的混合物(假定只含氯化钾一种钾盐)于烧杯中,用蒸馏水充分洗涤、过滤、干燥,固体质量减少了0.43g,在固体中继续加入过量的稀硫酸,微热让其充分反应,固体完全溶解得到的溶液中加入过量的NaOH溶液,经过滤、洗净、干燥,再在空气中充分灼烧得6.0 g棕色固体。求该加热材料反应前,铁和高氯酸钾的质量。(写出计算过程,结果保留2位有效数字)。
(14分)甲醇(CH3OH)和二甲醚(CH3OCH3)被称为21世纪的新型燃料。以CH4和H2O为原料制备二甲醚和甲醇的工业流程如下
(1)写出催化反应室1中在一定条件下进行的化学方程式:。
(2)在压强为0.1MPa条件下,反应室3(容积为VL)中amolCO与2amolH2在催化剂作用下反应生成甲醇:CO(g) +2H2(g) CH3OH(g),CO的平衡转化率与温度、压强的关系如图所示,
CH3OH(g),CO的平衡转化率与温度、压强的关系如图所示,
则:①P1P2。(填“<”、“>”或“=”)
②在其它条件不变的情况下,反应室3再增加a mol CO与2a mol H2,达到新平衡时,CO的转化率。(填“增大”、“减小”或“不变”)
③在P1压强下,100℃时,反应:CH3OH(g) CO(g)+2H2(g)的平衡常数为。(用含a、V的代数式表示)。
CO(g)+2H2(g)的平衡常数为。(用含a、V的代数式表示)。
(3)下图为绿色电源“二甲醚燃料电池”的工作原理示意图,a电极的电极反应式为。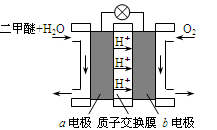
(4)水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g) CH3OH(g);ΔH=-90.8 kJ·mol-1
CH3OH(g);ΔH=-90.8 kJ·mol-1
②2CH3OH(g) CH3OCH3(g)+H2O(g);ΔH=-23.5kJ·mol-1
CH3OCH3(g)+H2O(g);ΔH=-23.5kJ·mol-1
③CO(g)+H2O(g) CO2(g) + H2(g);ΔH=-41.3 kJ·mol-1
CO2(g) + H2(g);ΔH=-41.3 kJ·mol-1
则反应:3H2(g) +3CO(g) CH3OCH3(g)+CO2(g)的ΔH=。
CH3OCH3(g)+CO2(g)的ΔH=。