用脱脂棉包住0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴几滴水,可观察到脱脂棉剧烈燃烧起来。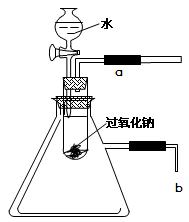
(1)由上述实验现象可得出两条有关过氧化钠跟水反应的结论是:
第一: ;第二: 。
(2)某研究性学习小组拟用如下图所示的装置进行实验,
以验证上述结论。
用以验证第一条结论的实验操作是 现象是 。
为了验证第二条结论,将管口b浸入水中,可观察到的现象为 。
欲配制100 mL 1.0 mol·L-1 Na2SO4溶液,正确的方法是( )
①将14.2 g Na2SO4溶于100 mL水中 ②将32.2 g Na2SO4·10H2O溶于少量水中,再用水稀释至100 mL ③将20 mL 5.0 mol·L-1 Na2SO4溶液用水稀释至100 mL
| A.①② |
| B.②③ |
| C.①③ |
| D.①②③ |
为了将混有Na2SO4、NaHCO3的NaCl提纯,并制得纯净的NaCl溶液,某学生设计了如图所示的实验方案:
(1)操作①盛放药品可选用________。(填仪器名称)
(2)操作②为什么不用Ba(NO3)2溶液,其理由是
________________________________________。
(3)进行操作②后,如何判断SO 已除尽?方法是________________________________。
已除尽?方法是________________________________。
(4)操作③的目的是_______;为何不先过滤后加Na2CO3溶液,其理由是________________。
(5)此设计方案是否严密?请说明理由________________。
氯化钠样品中含有少量的Na2SO4和Na2CO3,按下列流程进行净化。
(1)请在流程中的( )中写上合适的试剂,在[ ]中写上实验操作名称。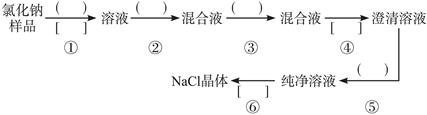
(2)写出有关反应的化学方程式:
第②步________________
第③步________________
第⑤步________________
有A、B、C三瓶失去标签的无色溶液:K2CO3、BaCl2、NaSO4。将它们分别与H2SO4作用,A产生白色沉淀,B产生无色气体,C中无明显现象。则A是________,B是________, C是________。
下列混合物的分离方法不可行的是( )
| A.互溶的液体混合物可以用分液的方法进行分离 |
| B.互不相溶的液体混合物可以用分液的方法进行分离 |
| C.沸点不同的混合物可以用蒸馏的方法进行分离 |
| D.可溶于水的固体与难溶于水的固体的混合物可用溶解、过滤的方法进行分离 |