铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备氧化铝的主要原料。工业上提取氧化铝的工艺流程如下: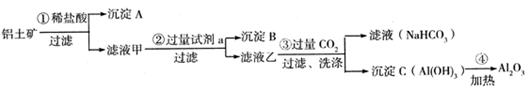
(1)沉淀 A、B的成分分别是 、 ;
(2)步骤②中的试剂a是 ;
(3)试写出步骤③中发生反应的离子方式 ;
(4)准确称取6g铝土矿样品,加入100mL盐酸溶液,充分反应后向滤液中加入10 mol·L-1试剂a的溶液,产生沉淀的质量与加入试剂a的体积关系如下图所示,则所用盐酸溶液的物质的量浓度为 ,样品中Al2O3的百分含量为 。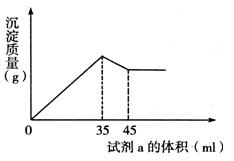
某一元弱酸(用HA表示)在水中的电离方程式是:HA H++A-,回答下列问题:
H++A-,回答下列问题:
(1)向溶液中加入适量NaA固体, 以上平衡将向______(填“正”、“逆”)向移动,理由是______________________。
(2)若向溶液中加入适量NaCl溶液,以上平衡将向____(填“正”、“逆”)向移动,溶液中c(HA)将________(填“增大”、“减小”或“不变”),溶液中c(OH-)将______(填“增大”、“减小”或“不变”)。
(3)试设计实验方案证明HA为弱酸_______________________________________。
(1)图1装置发生反应的离子方程式为。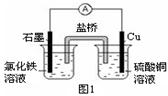
(2)图2装置中甲烧杯盛放100 mL 0.2 mol·L-1的NaCl溶液,乙烧杯盛放100 mL 0.5 mol·L-1L的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞溶液,观察到石墨电极附近首先变红。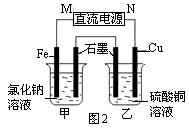
① 电源的M端为极,甲烧杯中铁电极的电极反应为。
② 乙烧杯中电解反应的化学方程式为。
③ 停止电解,取出Cu电极,洗涤、干燥、称量、电极增重 0.64 g,甲烧杯中产生的气体标准状况下体积为mL 。
(3)图3是甲醇燃料电池(电解质溶液为KOH溶液)结构示意图,写出 b处的电极反应式,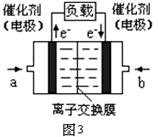
甲醇燃料电池的总反应化学方程式。
(1)家用液化气的主要成分之一是丁烷(C4H10),当2 mol丁烷完全燃烧生成二氧化碳和液态水时,放出热量为5800kJ,试写出表示丁烷燃烧热的热化学方程式:;
(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)="=" 2Fe(s)+3CO2(g)ΔH =" -24.8" kJ·mol-1
3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g)ΔH =" -47.4" kJ·mol-1
Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) △H =" +640.5" kJ·mol-1
写出CO(g)还原FeO(s)得到Fe (s)和CO2(g)的热化学反应方程式。
(12分) (1)某温度下,Kw=10-12。
①若保持温度不变,某溶液中c(H+)为1×10-7mol·L-1,则该溶液显性(填“酸”、“碱”或“中”)。
②若保持温度不变,向水中通入的HCl气体恰好使溶液中c(H+)/c(OH-)=1010,则此时水电离的c(H+)=mol·L-1。
(2)常温下,如果取0.1mol/LHA溶液与0.1mol/LNaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,试回答以下问题:
①混合溶液的pH=8的原因(用离子方程式表示):。
②混合溶液中离子浓度由大到小的顺序是:。
③混合溶液中由水电离出的c(H+)同浓度NaOH溶液中由水电离出的c(H+)
(填“>”、“<”或“=”)。
④求出混合溶液中下列算式的精确计算结果(填具体数据):
c(Na+)-c(A-)=mol/L。
(12分)在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2(g) 2SO3(g)ΔH<0
2SO3(g)ΔH<0
(1)写出该反应的化学平衡常数表达式:K=。
(2)降低温度,该反应K值,二氧化硫转化率,化学反应速率(以上均填“增大”、“减小”或“不变”)。
(3)600℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如下图所示,反应处于平衡状态的时间段是。
(4)据图判断,反应进行至20min时,曲线发生变化的原因是(用文字表达),10min~15min的曲线变化的原因可能是(填写编号)。
a.加了催化剂 b.扩大容器体积 c.降低温度 d.增加SO3的物质的量