高铁酸钾是一种高效的多功能的水处理剂。工业上常采用NaClO氧化法生产,原理为:
3NaClO + 2Fe(NO3)3 + 10NaOH=2Na2FeO4↓+ 3NaCl + 6NaNO3 + 5H2O
Na2FeO4+2KOH=K2FeO4+2NaOH
主要的生产流程如下:
(1)写出反应①的离子方程式_____________________________。
(2)流程图中“转化”是在某低温下进行的,说明此温度下Ksp(K2FeO4) _________ Ksp(Na2FeO4)(填“>”或“<”或“=”)。
(3)反应的温度、原料的浓度和配比对高铁酸钾的产率都有影响。
图1为不同的温度下,Fe(NO3)3不同质量浓度对K2FeO4生成率的影响;
图2为一定温度下,Fe(NO3)3质量浓度最佳时,NaClO浓度对K2FeO4生成率的影响。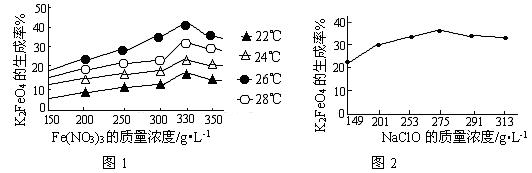
①工业生产中最佳温度为_______℃,此时Fe(NO3)3与NaClO两种溶液最佳质量浓度之比为_______。
②若NaClO加入过量,氧化过程中会生成Fe(OH)3,写出该反应的离子方程式:
____________________________________________________。
若Fe(NO3)3加入过量,在碱性介质中K2FeO4与Fe3+发生氧化还原反应生成K3FeO4,此反应的离子方程式:____________________________________。
(4)K2FeO4 在水溶液中易水解:4FeO42—+10H2O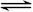 4Fe(OH)3+8OH—+3O2↑。在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用_______溶液(填序号)。
4Fe(OH)3+8OH—+3O2↑。在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用_______溶液(填序号)。
| A.H2O | B.CH3COONa、异丙醇 | C.NH4Cl、异丙醇 | D.Fe(NO3)3、异丙醇 |
在标准状况下,取甲、乙、丙各30.0mL 相同浓度的盐酸,然后分别慢慢加入组成相同的镁铝合金粉末,得下表中有关数据(假设反应前后溶液体积不发生变化):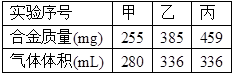
请回答:
(1)甲组实验中,盐酸(选填“过量”、“适量”或“不足量”,下同)__________________;乙组实验中盐酸______________。
(2)盐酸的物质的量浓度为_____________。
(3)合金中Mg. Al 的物质的量之比为_______________。
下表是元素周期表的一部分, 针对表中的①~⑩种元素,填写下列空白:(无特殊说明均填元素符号、化学式等化学用语)
| 主族 周期 |
IA |
ⅡA |
IIIA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0族 |
| 1 |
① |
|||||||
| 2 |
② |
③ |
④ |
|||||
| 3 |
⑤ |
⑥ |
⑦ |
⑧ |
⑨ |
|||
| 4 |
⑩ |
(1)在这些元素中,化学性质最不活泼的元素名称是,元素原子半径最小的是,⑧号元素的离子结构示意图为。
(2)在上述元素的最高价氧化物对应水化物中,酸性最强的化合物的化学式是,碱性最强的化合物的化学式是,既能与强酸反应,又能与强碱反应的化合物的化学式是。
(3)⑧、⑨号元素的氢化物中还原性较强的是(填化学式)。
(4)⑦的最高价氧化物与⑤的最高价氧化物对应的水化物反应的化学方程式为:_______。
(5)写出能说明⑨的非金属性比⑧强的一个实验事实________________________________。
四种短周期元素在周期表中的相对位置如下所示,其中Z元素原子核外电子总数是其最外层电子数的3倍。请回答下列问题:
(1)元素Z位于周期表中的位置________________________。
(2)这些元素的氢化物中,水溶液碱性最强的是______(填写化学式,下同);X、Y、Z三种元素的最高价氧化对应水化物中酸性由强到弱依次为________>_______>_________。
(3)Y的气态氢化物和其最高价氧化物对应的水化物相互反应的离子方程式为;_________。
(4)W和Y形成的一种二元化合物具有色温效应,其相对分子质量在170~190之间,且W的质量分数约为70%.该化合物的化学式为______。
(5)写出Y的最高价氧化物对应水化物的浓溶液与X在加热条件下反应的化学方程式_________,反应中若转移12mol电子,消耗的还原剂质量为________g。
(1)写出表示含有8个质子,10个中子的原子的化学符号:。
(2)最外层电子数为次外层电子数1/2的原子或;(填元素符号)
(3)根据下列微粒回答问题:1 1H、2 1H、3 1H、14C、14N、16O、35Cl2、37Cl2。
①以上8种微粒共有种核素,共种元素。
②互为同位素的是。
③质量数相等的是和,中子数相等的是和。
(4)相同物质的量的14CO2与S18O2的质量之比为;中子数之比为;电子数之比为。
A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出)。
(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,F的浓溶液与A、D反应都有红棕色气体生成,则A的原子结构示意图为________,反应①的化学方程式为__________________,反应④的化学方程式为________________。
(2)若A是常见的变价金属的单质,D、F是气态单质,且反应①在水溶液中进行。反应②也在水溶液中进行,反应②的离子方程式是_____________________________________.
(3)若A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式为___________________________________。