Ⅰ.已知某溶液中只存在OH-、H+、Na+、CH3COO-四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
①c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
②c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
③c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
④c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
填写下列空白:
(1)若溶液中溶解了一种溶质,则该溶质是______ ________,则该溶液中四种离子浓度的大小顺序符合上述4种关系中的______________。(填序号)
________,则该溶液中四种离子浓度的大小顺序符合上述4种关系中的______________。(填序号)
(2)若溶液中溶解了两种溶质,如果上述关系①是正确的,则溶液中的溶质 为__________;如果上述关系②是正确的,则溶液中的溶质为______________。
为__________;如果上述关系②是正确的,则溶液中的溶质为______________。
(3)若该溶液是由体积相等的NaOH溶液和醋酸混合而成,且恰好呈中性,则混合前c(NaOH) ______________c(CH3COOH)(填“大于”、“小于”、或“等于”,下同),混合后溶液中c(CH3COO-)______________c(Na+)。
Ⅱ.1919年,Langmuir提出等电 子原理:原子数相同、电子数相同的分子,互称为等电子体。等电子体的结构相似、物理性质相近。
子原理:原子数相同、电子数相同的分子,互称为等电子体。等电子体的结构相似、物理性质相近。
(1)根据上述原理,仅由第2周期元素组成的共价分子中,互为等电子体的是:
和 ; 和 。
(2)此后,等电子原理又有所发展。例如,由短周期元素组 成的微粒,只要其原子数相同,各微粒最外层电子数之和相同,也可互称为等电子体,它们也具有相似的结构特征。在短周期元素组成的物质中,与
成的微粒,只要其原子数相同,各微粒最外层电子数之和相同,也可互称为等电子体,它们也具有相似的结构特征。在短周期元素组成的物质中,与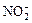 互为等电子体的分子有: 、 。
互为等电子体的分子有: 、 。
(3) CNS-、NO2+具有相同的通式:AX2,它们的价电子总数都是16,因此,它们的结构与由第二周期两元素组成的 分子的结构相同(填化学式),微粒构型呈
形。
(1)已知在K2Cr2O7的溶液中存在如下平衡: Cr2O72-(橙色)+H2O 2CrO42-(黄色)+2H+,向5mL0.1mol/L K2Cr2O7溶液中滴加3-10滴浓H2SO4,观察到的现象为__________;在此基础上再滴加5-10滴6mol/LNaOH溶液,溶液颜色变化为__________。
2CrO42-(黄色)+2H+,向5mL0.1mol/L K2Cr2O7溶液中滴加3-10滴浓H2SO4,观察到的现象为__________;在此基础上再滴加5-10滴6mol/LNaOH溶液,溶液颜色变化为__________。
(2)已建立平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动时,下列叙述正确的是__________(填序号)。
①生成物的产量一定增加
②生成物的体积分数一定增加
③反应物的浓度一定降低
④反应物的转化率一定增加
⑤正反应速率一定大于逆反应速率
(7分)现有一包固体粉末,可能是CaCO3、Na2CO3、Na2SO4、CuSO4、NaCl中的一种或几种,为确定其组成,取适量试样进行下列实验.请根据实验现象判断:
(1)取试样溶于水,得到无色澄清溶液,则此固体粉末中一定没有______、______。
(2)取上述溶液适量,滴加过量的BaCl2溶液,出现白色沉淀,再加入过量的稀硝酸,沉淀部分消失并产生气泡.则此固体粉末中一定有______、______。
(3)取步骤(2)实验后的上层清液,加入稀硝酸、硝酸银溶液,出现白色沉淀,由此该同学得出此固体粉末中一定含有NaCl,你认为此结论是否正确______(填“是”或“否”).
(4)对于是否含有NaCl,你认为应对步骤(2)作如何改进(若步骤(3)填“是”,此空不作答)。
漂白粉在生活、工业生产中用途广泛,漂白粉除了具有漂白作用外,还能杀菌消毒。2003年抗“非典”期间,各商场漂白粉及其他漂白产品曾一度脱销。
(1)1998年,我国长江流域和松花江流域都发生了百年不遇的特大洪水。灾区人民的饮用水,必须用漂白粉等药品消毒后才能饮用,以防传染病发生,但瓶装漂白粉久置空气中会失效。试用化学方程式表示漂白粉在空气中易失效的原因:
①②。
(2)已知浓盐酸和次氯酸钙能发生如下反应:Ca(ClO)2 +4HCl(浓)===CaCl2+2Cl2↑+2H2O
用贮存很久的漂白粉与浓盐酸制得的氯气中,可能有的杂质气体是()
①CO2②HCl③H2O④O2
A.①②③ B. ②③④ C.②③ D.①④
(3)用Cl2和石灰乳制作漂白粉的目的是()
A. 转变为较HClO稳定且易储运的物质 B. 转变为更易溶于水的物质
C. 提高氯气的利用率 D.增强漂白能力
(4)用Cl2和石灰乳制作漂白粉的反应方程式
其有效成分是(填名称)。
(4分)有四种物质是:标准状况下有①6.72LCH4;②3.01x1023个HCl;③13.6gH2S;④0.2molNH3,它们中物质的量最大的是,所含分子数最多的是,含有原子数最多的是,质量最大的是。(用序号填空)
(8分)(1)给下列方程式配平,用双线桥标电子转移方向和数目
MnO2 +HCl(浓) = MnCl2 + Cl2↑ +H2O 当发生转移的电子物质的量0.5摩时,被氧化的HCl物质的量为。
(2)亚铁盐容易与空气中的氧气发生氧化还原反应而变质,在配制亚铁盐溶液时往往要加入适量的铁粉防止变质,氧气在亚铁盐变质中做为(填氧化剂或还原剂,下同),加入铁粉在防止变质时是做为。