纳米材料二氧化钛(TiO2)可做优良的催化剂。
| 资料卡片 |
|
|
| 物质 |
熔点/℃ |
沸点/℃ |
| SiCl4 |
-70 |
57.6 |
| TiCl4 |
-25 |
136.5 |
Ⅰ. 工业上二氧化钛的制备方法:
① 将干燥后的金红石(主要成分为TiO2,主要杂质SiO2)与碳粉混合装入氯化炉中,在高温下通入Cl2反应,制得混有SiCl4杂质的TiCl4。
② 将SiCl4分离,得到纯净的TiCl4。
③ 在TiCl4中加水、加热,水解得到沉淀TiO2·xH2O。
④ TiO2·xH2O高温分解得到TiO2。
(1) 根据资料卡片中信息判断,TiCl4与SiCl4在常温下的状态是____________,分离二者所采取的操作名称是________________。
(2) ③中反应的化学方程式是________________________________________________。
(3) 若④在实验室完成,应将TiO2·xH2O放在________________(填仪器名称)中加热。
Ⅱ. 据报道:能“吃废气”的“生态马路”是在铺设时加入一定量的TiO2,TiO2受太阳光照射后,产生的电子被空气或水中的氧获得,生成H2O2,其过程大致如下:
a. O2―→2O b. O+H2O―→2OH c. OH+OH―→H2O2
(4) b中破坏的是______________(填“极性共价键”或“非极性共价键”)。
(5) H2O2能清除路面空气中的CxHy、CO等,主要是利用了H2O2的____________(填“氧化性”或“还原性”)。
Ⅲ. 某研究性学习小组用下列装置模拟“生态马路”清除CO的原理。(夹持装置已略去)
(6) 若缓慢通入22.4L(已折算成标准状况)CO气体,结果NaOH溶液增重16.5g,则CO的转化率为___ _________。
_________。
(7) 当CO气体全部通入后,还要通一会儿空气,其目的是 。
已知SO2可以用Fe(NO3)3溶液吸收,某学习小组据此按下图装置展开如下相关探究:取一定量的铜片于三颈烧瓶中,通入一段时间N2后再加入足量的浓硫酸,加热。装置A中有白雾(硫酸酸雾)生成,装置B中产生白色沉淀。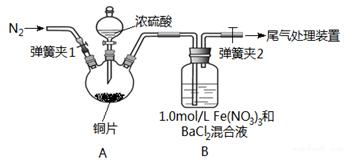
回答下列问题:
(1)装置A中用于添加浓硫酸的仪器名称为;检查图中连通装置A、B气密性的方法是。
(2)加入浓硫酸之前先通人N2一段时间,其目的是;排除装置A中白雾影响,可在装置A、B间增加洗气瓶C,则C中盛放的试剂是。若用氢氧化钠溶液处理尾气,则发生反应的离子方程式为。
(3)经过讨论,该小组对装置B中产生沉淀的原因,提出下列假设(不考虑各因素的叠加):
假设1:装置A中白雾进入装置B中参与了反应。
假设2:。
假设3:Fe(NO3)2溶液显酸性,在此酸性条件下NO3‾能氧化SO2。
(4)请你设计实验验证上述假设3,写出实验步骤、预期现象和结论。
| 实验步骤(简述操作过程) |
预期现象和结论 |
| ①测1.0mol•L‾1Fe(NO3)3溶液的pH; ② ③ ④ |
(13分)过氧化钙是一种新型的多功能无机化工产品,常温下是无色或淡黄色粉末,易溶于酸。难溶于水、乙醇等溶剂。某实验小组在实验室用钙盐制取Ca02·8H20沉淀(该反应是一个放热反应)。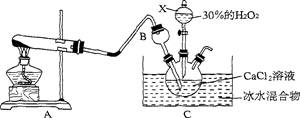
(1)仪器X的名称是。将装置A与B连接后要检查气密性,检查气密性的方法为
(2)仪器B的作用是。
(3)写出A中发生反应的化学方程式:。
(4)制取CaO2·8H20一般在0~5℃的低温下进行,原因是.生成CaO2·8H20的 化学方程式为。
(5)2.76 g CaO2·8H20样品受热脱水过程的热重曲线(样品质量随温度变化的曲线,140℃时完全脱水,杂质受热不分解)如图所示。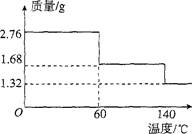
①试确定60℃时CaO2·xH20中x=。
②该样品中CaO2的质量分数为。
(15分)碱式碳酸钴 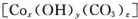 常用作电子材料、磁性材料的添加剂,受热时可分解生成三种氧化物。为了确定其组成,某化学兴趣小组同学设计了如图所示的装置进行实验。
常用作电子材料、磁性材料的添加剂,受热时可分解生成三种氧化物。为了确定其组成,某化学兴趣小组同学设计了如图所示的装置进行实验。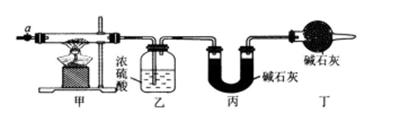
(1)请完成下列实验步骤:
①称取3.65 g样品置于硬质玻璃管内,称量乙、丙装置的质量;
②按如图所示装置组装好仪器,并检验装置气密性;
③加热甲中玻璃管,当乙装置中_______(填实验现象),停止加热;
④打开活塞a,缓缓通入空气数分钟后,称量乙、丙装置的质量;
⑤计算。
(2)步骤④中缓缓通人空气数分钟的目的是___________________________________.
(3)某同学认为上述实验装置中存在一个明显缺陷,为解决这一问题,可选用下列装置中的_______(填字母)连接在_______(填装置连接位置)。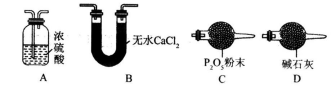
(4)若按正确装置进行实验,测得如下数据。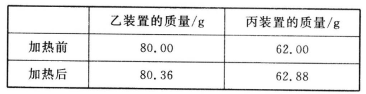
则该碱式碳酸钴的化学式为______________。
(5)含有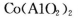 的玻璃常用作实验室观察钾元素的焰色反应,该玻璃的颜色为_______。
的玻璃常用作实验室观察钾元素的焰色反应,该玻璃的颜色为_______。
(6) 常用作多彩水泥的添加剂。以含钴废料(含少量Fe、Al等杂质)制取
常用作多彩水泥的添加剂。以含钴废料(含少量Fe、Al等杂质)制取 的一种工艺如下:
的一种工艺如下: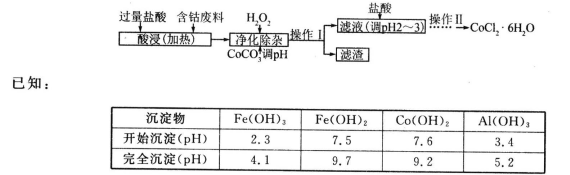
①净化除杂时,加入H2O2发生反应的离子方程式为____________________________.
②加入CoCO3调pH为5.2~7.6,则操作1获得的滤渣成分为_____________________.
③加盐酸调整pH为2~3的目的为__________________________________________.
④操作Ⅱ过程为蒸发浓缩、______________(填操作名称)、过滤。
(14分)某化学小组用下图所列装置(固定装置略)验证CO能还原CuO,并探究其还原产物的组成。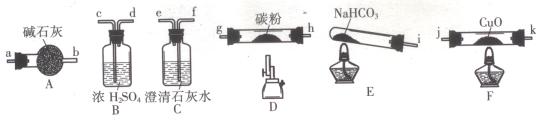
请回答:
(1)按气流方向,各装置从左到右的连接顺序为:
i→( )( )→( )( )→( )( )→( )( )→( )( )尾气处理(填仪器接口的字母编号)。
(2)说明CO能还原CuO的实验现象为___________________________。
(3)该实验处理尾气的方法为___________________________。
(4)若去掉B装置,可能产生的影响为___________________________。
(5)将各装置按正确的顺序连接后进行实验。当反应结束后,F处硬质玻璃管中的固体全部变为红色。
[查阅资料]Cu和Cu2O均为红色;Cu2O在酸性溶液中能生成Cu和Cu2+。
[提出猜想]红色固体的成分可能为:①Cu;②Cu2O;③________。
[实验验证]该小组为验证上述猜想,分别取少量红色固体放人试管中,进行如下实验。
| 实验编号 |
操作 |
现象 |
| a |
加入足量稀硝酸,振荡 |
试管内红色固体完全溶解,溶液变为蓝色,并有无色气体产生 |
| b |
加入足量稀硫酸,振荡 |
试管内有红色固体,溶液为无色 |
[实验评价]根据上述实验,不能确定红色固体成分的实验是________(填实验编号),理由为_________(用化学方程式表示)。
[实验结论]根据上述实验结果,可知红色固体的成分为________(填化学式)。
(15分)下列实验步骤是兴趣小组对某混合样品含量的测定,样品成分为FeO、FeS2、SiO2、及其它杂质,杂质不与酸碱反应,受热稳定。(步骤中所加试剂均为足量)
①称量m g样品灼烧。装置如下: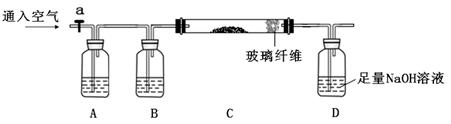
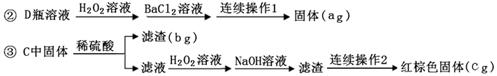
请回答下列问题:
(1)连接好仪器后,如何检查整套装置的气密性。
(2)A瓶内所盛试剂是溶液。灼烧完成后熄灭酒精灯,若立即停止通空气,可能对实验的影响是(写两点)。
(3)步骤②中加入双氧水的离子方程式为。若此步骤不加入双氧水对测定硫元素含量的影响是(填“偏高”、“偏低”或“无影响”) 。
(4)连续操作1为、洗涤、、称量;连续操作2为洗涤、、称量。
(5)从步骤③的b g滤渣入手,可测定SiO2的含量,下面各组试剂中不适合测定的是。
| A.NaOH溶液、稀硫酸 | B.Ba(OH)2溶液、盐酸 |
| C.氨水、稀硫酸 | D.NaOH溶液、盐酸 |
(6)求样品中FeO的质量分数(列出算式即可)。