某工业废水中仅含下表离子中的5种(不考虑水的电离及离子的水解),且各种离子的物质的量浓度相等,均为0.1mol/L。
| 阳离子 |
K+ Cu2+ Fe3+ Al3+ Fe2+ |
| 阴离子 |
Cl- CO32- NO3- SO42- SiO32- |
甲同学欲探究废水的组成,进行了如下实验:
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察)。
Ⅱ.取少量溶液,加入KSCN溶液无明显变化。
Ⅲ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变。
Ⅳ. 向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成。请推断:
(1)由Ⅰ、Ⅱ判断,溶液中一定不含有的阳离子是 (写离子符号)。
(2)Ⅲ中加入少量盐酸生成无色气体的的离子方程式是_________________________。
(3)将Ⅲ中所得红棕色气体通入水中,气体变无色,所发生的化学方程式为
_______________________________________________________________
(4)甲同学最终确定原溶液中所含阳离子是 ,阴离子是 。(写离子符号)
(5)另取100mL原溶液,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,得到的固体质量为 g。
(6)工业废水中常含有不同类型的污染物,可采用不同的方法处理。以下是乙同学针对含不同污染物的废水提出的处理措施和方法,其中正确的是__________
| 选项 |
污染物 |
处理措施 |
方法类别 |
| A |
废酸 |
加生石灰中和 |
物理法 |
| B |
Cu2+等重金属离子 |
加硫酸盐沉降 |
化学法 |
| C |
含复杂有机物的废水 |
通过微生物代谢 |
物理法 |
| D |
碱性的废水 |
用CO2来中和 |
化学法 |
亚硫酸钠是食品加工中广泛使用的漂白剂、防腐剂和抗氧化剂,其在食品中的残留量通常以二氧化硫含量计算。
(1)亚硫酸盐具有一定的毒性,长期摄入过量的亚硫酸盐,红细胞和血红蛋白会减少,钙的吸收也会减少,原因是。
检验某黑木耳中是否含有亚硫酸盐的简单方法是:将黑木耳样品剪成碎末放入烧杯,加入20mL水和10mL盐酸,加热一会儿,滴入试剂A,观察现象既可。
(2)加热的作用是,加热时间不能太长的原因是。
(3)试剂A是。
在足量的亚硫酸钠溶液中加入1~2滴液溴,振荡后溶液变为无色。
(4)写出以上反应的离子方程式 。
(5)以上反应后的溶液中含有SO32-、HSO3-、SO42-、Br-、OH-等阴离子。设计实验检验SO42- 和Br-,写出实验方法。试剂不限。
| 实验操作 |
预期现象与结论 |
| 步骤1: |
|
| 步骤2: |
工业上生产高氯酸(沸点:90oC)时还同时生产了亚氯酸钠,其工艺流程如下: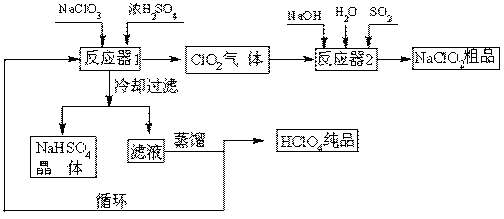
(1)冷却过滤的目的。
(2)通入反应器2的SO2作用是;反应器2中发生反应的离子方程式为。
(3)循环使用的物质是。
(4)可以通过蒸馏滤液的方法得到高氯酸的原因可能是。
(5)通过电解NaClO3水溶液的方法也可以制备NaClO4,进而可以制备HClO4,写出阳极的电极反应式。
氮化硅(Si3N4)是一种新型陶瓷材料,它可由SiO2与过量焦炭在1300-1700oC的氮气流中反应制得3SiO2(s)+6C(s)+2N2(g) Si3N4(s)+6CO(g)
Si3N4(s)+6CO(g)
(1)上述反应氧化剂是,已知该反应每转移1mole—,放出132.6kJ的热量,该方程式的∆H =。
(2)能判断该反应(在体积不变的密闭容器中进行)已经达到平衡状态的是()
A.焦炭的质量不再变化 B.N2和CO速率之比为1:3
C.生成6molCO同时消耗1mol Si3N4 D.混合气体的密度不再变化
(3)下列措施中可以促进平衡右移的是()
A.升高温度 B.降低压强
C.加入更多的SiO2 D.充入N2
(4)该反应的温度控制在1300-1700oC的原因是。
(5)某温度下,测得该反应中N2和CO各个时刻的浓度如下,求0—20 min内N2的平均反应速率,该温度下,反应的平衡常数K=。
| 时间/min |
0 |
5 |
10 |
15 |
20 |
25 |
30 |
35 |
40 |
45 |
| N2浓度/mol·L-1 |
4.00 |
3.70 |
3.50 |
3.36 |
3.26 |
3.18 |
3.10 |
3.00 |
3.00 |
3.00 |
| CO浓度/mol·L-1 |
0.00 |
0.90 |
1.50 |
1.92 |
2.22 |
2.46 |
2.70 |
— |
— |
— |
咖啡酸(见右),存在于许多中药中,如野胡萝卜、光叶水苏、荞麦、木半夏等。咖啡酸有止血作用,特别对内脏的止血效果较好。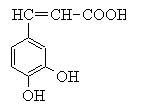
(1)咖啡酸的化学式是,咖
啡酸中含氧官能团的名称为 。
(2)咖啡酸发生加聚反应的化学方程式。
(3)下列关于咖啡酸的说法正确的是()
| A.1mol咖啡酸只与1mol溴反应 |
| B.咖啡酸有一种同分异构体的苯环上连4个羟基 |
| C.咖啡酸的水溶液中滴加氯化铁溶液显血红色 |
| D.可以用高锰酸钾或溴水检验咖啡酸分子中所含的碳碳双键 |
(4)写出1分子咖啡酸与2分子CH3COCl在一定条件下发生反应生成酯的方程式
。
(5)A是咖啡酸的一种同分异构体,A中苯环上的取代基仅1个,1molA能与2molNaHCO3反应,A的结构简式为。
反应① Fe(s)+CO2(g)===FeO(s)+CO(g);△H1=" a" kJmol-1
反应② CO(g)+1/2O2(g)===CO2(g);△H2=" b" kJmol-1
测得在不同温度下,在密闭容器中进行的反应①的平衡常数K值随温度的变化如下:
(1)反应①的化学平衡常数表达式为,a0(填“> ”、“<”或“="”)。" 在 500℃2L 密闭容器中进行反应①,Fe 和 CO2的起始物质的量均为4mol,10min后达到平衡状态,平衡时CO2的转化率为,用CO表示的化学反应速率为。
”、“<”或“="”)。" 在 500℃2L 密闭容器中进行反应①,Fe 和 CO2的起始物质的量均为4mol,10min后达到平衡状态,平衡时CO2的转化率为,用CO表示的化学反应速率为。
(2)700℃反应①到平衡,要使该平衡向右移动,其它条件不变时,可以采取的措施有(填序号)。
| A.缩小反应器体积 | B.通入CO2 | C.升高温度到900℃ | D.使用合适的催化剂 |
(3)下列图像符合反应①的是(填序号)(图中v是速率、 为混合物中CO的含量,T为温度)。
为混合物中CO的含量,T为温度)。
(4)由反应①和②可求得反应2Fe(s)+O2(g)===2FeO(s) △H3中的△H3=(用含a、b的代数式表示)。
(5)如下图是甲醇燃料电池(电解质溶液为KOH溶液)的结示意图,则a处通入的是
(填“甲醇”或“氧气”),b处电极上发生的电极反应是: