某电镀铜厂有两种废水需要处理,一种废水中含有CN-离子,另一种废水中含有Cr2O72-离子。该厂拟定如图所示的废水处理流程。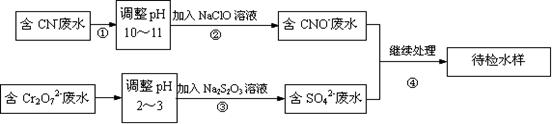
回答以下问题:
(1)上述处理废水的流程中主要使用的方法是 。
(2)②中使用的NaClO溶液呈碱性,用离子方程式解释原因  。
。
(3)②中反应后无气体放出,该反应的离子方程式为 。
(4)③中反应时,每0.4 molCr2O72-转移2.4 mol的电子,该反应的离子方程式为 。
(5)取少量待检水样于试管中,先加入NaOH溶液,观察到有蓝色沉淀生成,继续加入NaOH溶液,直到不再产生蓝色沉淀为止,再加入Na2S溶液,有黑色沉淀生成,且蓝色沉淀逐渐减少。请你使用化学用语,结合必要的文字解释其原因 。
(选做题)图表法、模型法是常用的科学研究方法。
I.下图是研究部分元素的氢化物的沸点变化规律的图像。不同同学对某主族元素氢化物的沸点的变化趋势画出了两条折线——折线a和折线b(其中A点对应的沸点是100℃),你认为正确的是,理由是。
II.人类在使用金属的历史进程中,经历了铜、铁、铝之后,第四种将被广泛应用的金属则被科学家预测为是钛(Ti)。钛被誉为“未来世纪的金属”。试回答下列问题:
(1)22Ti元素基态原子的价电子层排布式为。
(2)在Ti的化合物中,可以呈现+2、+3、+4三种化合价,其中以+4价的Ti最为稳定。偏钛酸钡的热稳定性好,价电常数高,在小型变压器、话筒和扩音器中都有应用。偏钛酸钡晶体中晶胞的结构示意图如右图,则它的化学式是。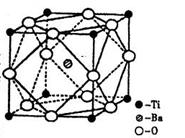
III.上世纪60年化,第一个稀有气体化合物Xe[PtF6]被合成出来后,打破了“绝对情性”的观念。在随后的几年内,科学家又相继后成了氙的氟化物、氧化物等。
(1)金属Pt内部原子的堆积方式与铜及干冰中的CO2相同,右图正方体是Pt晶胞的示意图,试说出Pt原子在晶胞中的位置。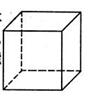
(2)稀有气体(氡除外)中,只有较重的氙能合成出多种化合物,
其可能原因是(填字母代号)
| A.氙的含量比较丰富 | B.氙的相对原子质量大 |
| C.氙原子半径大,电离能小 | D.氙原子半径小,电负性大 |
(3)已知XeO3分子中氙原子上有1对弧对电子,则XeO3为分子(填“极性”或“非极性”)。
(选做题)下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
试回答下列问题:
(1)元素p为26号元素,请写出其基态原子电子排布式。
(2)d与a反应的产物的分子中中心原子的杂化形式为。
(3)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:。
(4)o、p两元素的部分电离能数据列于表:
| 元素 |
o |
P |
|
| 电离能/kJ·mol-1 |
I1 |
717 |
759 |
| I2 |
1509 |
1561 |
|
| I3 |
3248 |
2957 |
比较两元素的I2、I3可知,气态o2+再失去一个电子比气p2+再失去一个电子。对此,你的解释是。
(5)i单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示,则晶胞中i原子的配位数为。
(6)元素a、c、e可形成一种相对分子质量为60的一元羧酸分子,其分子中共形成个 键,个
键,个 键。
键。
(7)第三周期8种元素按单质熔点高低的顺序如下图,其中电负性最大的是(填下图中的序号)。
(8)短周期某主族元素M的电离能情况如下图所示,则M元素是述周期表的元素(填元素符号)。
(1)甲烷是一重要的清洁能源、请写出以KOH溶液为电解质溶液,甲烷燃料电池的正极反应式:。
(2)电解原理在化学工业中有广泛的应用。图中a为电解液,X和Y是两块电极板,则:
①若X和Y分别为铁和石墨,a为饱和食盐水,则电解时X电极反应式为。
②若X、Y分别为石墨和铁,a为饱和食盐水,则电解过程中生成的白色固体露置在空气中,可观察到的现象是。
(3)高纯铜(纯度可达99.99%)广泛应用于电器工业。某粗铜样品中含Fe、Ni、Ag、Au等四种金属杂质,可用电解法进行精炼制得高纯铜。电解完毕后,某兴趣小组欲对电解溶中的离子进行分离,他们通过查阅资料,得知相关氢氧化物在不同pH下的溶解度曲线如下图。
①结合右图分析,相同温度下Kap[Cu(OH)2]、Kap[Ni(OH)2]、Kap[Fe(OH)2]由大到小的顺序为。
②分离过程中,使上述溶液的pH逐渐增加,则溶液中的Cu2+、Fe2+和Ni2+沉淀的先后顺序依次为(填写离子符号)。
CO是重要的化工原料,应用十分广泛。
(1)已知: C(s)+O2(g)CO2(g)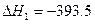 kJ·mol-1
kJ·mol-1
C(a)+H2O(g)CO(g)+H2(g)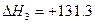 kJ·mol-1
kJ·mol-1
则反应CO(g)+H2(g)+O2(g)H2O(g)+CO2(g)的 。
。
(2)在10L密闭容器中充有10 molCO 与20molH2,在催化剂作用下反应生成甲醇:
CO(g)+2H2(g) 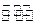 CH3OH(g);CO的转化率(
CH3OH(g);CO的转化率(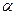 )与温度、压强的关系如右图所示。
)与温度、压强的关系如右图所示。
①若A、B两点表示在某时刻达到的平衡状态,则在A点该温度下的平衡常数K=。
②若A、C两点都表示达到平衡状态,则自反应开始到达平衡状态所需的时间tAtC(填“大于”、“小于”或“等于”)。
(3)室温下,向一定量的稀氨水中逐滴加入浓度相同的稀盐酸。
①当溶液中离子浓度关系满足c(NH4+)<(Cl-)时,则反应的情况可能为(填写序号字母)
A.盐酸不足,氨水剩余,溶液显碱性
B.氨水与盐酸恰好完全反应
C.盐酸过量
②当溶液的pH为7时,溶液中各离子浓度的大小关系为。
③实验过程中,氨水中的溶2O的电子离程度先后(填“增大”、“减小”或“不变”)。
测定慕硫酸锄黑体(Na2SO4·XH2O)中结晶水含量韵实验包括如下两步:
①将硫酸钠晶体制成粉末,准确称取该样品26.8 g
②将样品加热至恒重,冷却后称得样品质量变为14.2 g
试回答下列问题:
(1)将晶体制成粉末,所用的主要化学仪器是____(填仪器名称,下同);准确称量后将样品放在中加热至恒重。
(2)判断试样已加热至恒重的标准是________。
(3)根据实验数据计算出x=____。
(4)下面的情况有可能造成测定结果偏低的是(填序号)。
| A.试样中含有加热易挥发的杂质 | B.加热后不是在于燥器中冷却试样 |
| C.实验前坩埚来完全干燥 | D.加热时有晶体溅出 |
E.试样中含有加热不挥发的杂质