Fe2O3和Cu2O都是常用的红色颜料。某红色粉末可能含有Fe2O3和Cu2O,某化学实验小组通过实验来探究该红色粉末的成分。已知:Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4,在空气中加热生成CuO。
(1)提出假设 假设1:红色粉末只含Fe2O3;
假设2:_______________________________;
假设3:红色粉末是Fe2O3和Cu2O的混合物。
(2)初步探究: 取少量红色粉末于小烧杯中,放入足量稀硫酸,充分搅拌后粉末全部溶解(温馨提示:Cu+2Fe3+=Cu2++2Fe2+)。上述三个假设中,可能成立的是___________ 。
(3)进一步探究:完成后续实验方案的设计,填写下表中实验步骤、预期实验现象和结论(可不填满,也可补充)。
限选实验试剂:3 mol·L—1 H2SO4、3 mol·L—1 NaOH、0.01 mol·L—1 KMnO4、20% KSCN、3%H2O2、淀粉-KI溶液。
| 实验步骤 |
预期现象和结论 |
| |
|
(12分)某混合物的水溶液,可能含有以下离子中的若干种:K+、NH4+、Al3+、Ba2+、CO32-、SO42-、Cl-、Br-。现分别取100 mL的三等份溶液进行如下实验:
①第一份加过量浓NaOH溶液加热后,收集到气体0.02 mol,无沉淀生成,同时得到溶液甲。再向甲溶液中通人过量的CO2,生成白色沉淀,沉淀经过滤、洗涤、干燥、灼烧后,得到1.02 g固体。
②第二份加足量盐酸酸化的BaC12溶液,经过滤、洗涤、干燥后,得到沉淀的质量为11.65 g,
③第三份加CCl4,滴加少量氯水,振荡后静置, CCl4层未变红色;
依据实验回答下列问题:
(1)分析上述实验,写出每一实验可以确定离子一定存在或不存在的种类。
实验①可以确定:一定存在的离子有__________,一定不存在的离子有___________;
实验②可以确定:一定存在的离子有___________________,一定不存在的离子有________;
实验③可以确定:一定不存在的离子有_____________________。
(2)试通过分析与计算,原溶液中K+的物质的量浓度为____________mol·L-1。
下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题: 
(1)装置B中①的名称是,若用CCl4来萃取碘水中的碘,静置后,碘的CCl4溶液在层,呈色;回收碘的CCl4溶液中的CCl4选择装置__ _ ___(填代表装置图的字母)。
(2)为除去粗盐中的Ca2+、Mg2+、SO以及泥沙等杂质,某同学利用相关装置设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
Ⅰ.步骤①的操作名称是 ▲ 。
Ⅱ.第④步中,加入的试剂是__ ▲____(填化学式),该步骤中涉及的离子反应方程式为:
__ ▲__ __, ▲。
Ⅲ.判断第⑥步盐酸已“适量”的方法是__ ▲__ __。
Ⅳ.假设按照上述流程准确规范完成后,最后得到的精盐固体的质量为m1;若没有进行第⑥步,第⑤步完成后直接进行第⑦步得到的精盐固体质量为m2;则m1__ ▲__ __m2。(填“大于”或“小于”或“等于”)
氮化铝(AlN)是一种新型无机材料,广泛应用于集成电路生产领域。某化学研究小组利用Al2O3+3C+N2 2AlN+3CO制取氮化铝,设计下图实验装置:
2AlN+3CO制取氮化铝,设计下图实验装置: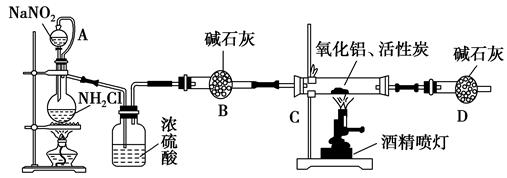
试回答:
(1)实验中用饱和NaNO2与NH4Cl溶液制取氮气的化学方程式为。
(2)装置中分液漏斗与蒸馏烧瓶之间的导管A的作用是________(填写序号)。
a.防止NaNO2饱和溶液蒸发 b.保证实验装置不漏气 c.使NaNO2饱和溶液容易滴下
(3)按图连接好实验装置,检查装置气密性的方法是________________。
(4)化学研究小组的装置存在严重问题,请说明改进的办法________________。
(5)反应结束后,某同学用图装置进行实验来测定氮化铝样品的质量分数(实验中导管体积忽略不计)。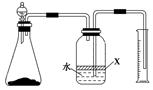
已知:氮化铝和NaOH溶液反应生成NaAlO2和氨气。
①广口瓶中的试剂X最好选用________(填写序号)。
a.汽油b.酒精c.植物油d.CCl4
②广口瓶中的液体没有装满(上方留有空间),则实验测得NH3的体积将________(填“偏大”、“偏小”或“不变”)。
③若实验中称取氮化铝样品的质量为10.0 g,测得氨气的体积为3.36 L(标准状况),则样品中AlN的质量分数为________。
(共12分)
MnO2是一种重要的无机功能材料,粗MnO2的提纯是工业生产的重要环节。某研究性学习小组设计了将粗MnO2(含有较多的MnO和MnCO3)样品转化为纯MnO2实验,其流程如下:
(1)第①步加稀H2SO4时,粗MnO2样品中的(写化学式)转化为可溶性物质。
(2)第②步反应的离子方程式是
□+ □ClO3— + □= □MnO2↓ + □Cl2↑ + □。
(3)第③步蒸发操作必需的仪器有铁架台(含铁圈)、酒精灯、、。
已知蒸发得到的固体中含有NaClO3和NaOH,则一定还含有(写化学式)。
(4)用浓硫酸来配制本实验需要的稀硫酸,进行如下操作,其中会使所配溶液浓度偏高的是
A用量筒量取浓硫酸倒入小烧杯后,用蒸馏水洗涤量筒并将洗涤液转移到小烧杯中
B定容时仰视
C用量筒量取浓硫酸时,读数时仰视
D容量瓶中有水,未进行干燥
(5)若粗MnO2样品的质量为12.69g,第①步反应后,经过滤得到8.7g MnO2,并收集到0.224L CO2(标准状况下),则在第②步反应中至少需要mol NaClO3。
二氯化硫(SCl2)熔点-78℃,沸点59℃。密度1.638 g·cm-3,遇水易分解,是一种重要的化工试剂,下图是氯气与硫在50~59℃时合成二氯化硫的实验装置。
(1)装置A中发生反应的化学方程式为:。
(2)装置B盛放的药品是,作用是;装置C盛放的药品是,作用是。
(3)实验开始前先在D中放入一定量的硫粉,加热使硫熔化,然后转动和摇动烧瓶使硫附着在烧瓶内壁表面形成一薄层,这样做的目的是。
(4)F装置中干燥管内所盛物质是,一个作用是,还有一个作用是。