按要求完成下列各小题:
(1)我国古代四大发明之一的黑火药,爆炸时的反应为S+2KNO3+3C=K2S+N2↑+3CO2,该反应中还原剂是,氧化剂是。
(2)制普通玻璃的原料是,其中是制水泥和普通玻璃的共同原料。
(3)用氧化物的形式表示某硅酸盐的组成:K4Al4FeSi6O18(OH)7.
(4)漂白粉的成分是,工业制漂白粉的化学方程式为漂白粉在空气中保存不当会失效的原因,用化学方程式表示
(5)将23gNa与28g硅同时投入水中,理论上放出H2g,写出反应中有关的离子方程式。
已知A——H有下列转化关系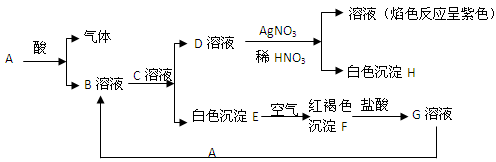
(1)与A反应的酸的名称:
(2)写出E转变成F的化学方程式:
(3)写出D与AgNO3溶液反应的化学方程式:
(4)写出G溶液与A反应的离子方程式
(5)鉴别G溶液常用的试剂是:
如图所示,各项变化的未知物焰色的反应均为黄色,E为淡黄色粉末,据此回答下列问题: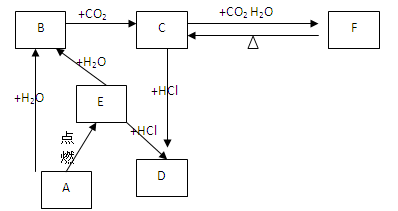
(1)写A→E的化学方程式,标出电子转移的方向和数目。
(2)写出C→D的离子方程式。
(3)在B→C的变化中,所得C的溶液往往不纯,其中的杂质(不包括水)可能是,主要原因是,还可能是,主要原因是。
今有13种物质:①铝线②单质硅③Na2O④液氯⑤盐酸⑥乙醇⑦熔融的KNO3⑧漂白粉⑨CO2⑩NH3⑾水玻璃(12)BaSO4 (13)SO2
(1)能导电的是。(用物质前的序号回答,下同)
(2)属于电解质的是。
(3)属于非电解质的是。
(4)既不是电解质又不是非电解质的是。
某研究性学习小组利用手持技术探究强碱和不同的酸中和反应的过程如下:
(1)实验步骤:
①分别配制浓度均为0.1mol·L-1的NaOH、HC1、CH3 C00H、H3PO4溶液备用。配制过程中用到的玻璃仪器有烧杯、容量瓶、玻璃棒、细口瓶、____、____。
②在锥形瓶中加入10mL0.1 mol.L-1的HC1,在25.00mL____(填“酸式”、“碱式”)滴定管中加入0.1 mol.L-1的NaOH,连接数据采集器和pH传感器。
③向锥形瓶中滴入NaOH,接近估算的NaOH用量附近时,减慢滴加速度,等读数稳定后,再滴下一滴NaOH。
④存储计算机绘制的pH变化图。用0.1 mol·L-1的CH3 C00H、H3 P04溶液代替HC1重复上述②~④的操作。
(2)结果分析:20℃时NaOH分别滴定HC1、CH3 C00H、H3 P04的pH变化曲线如下。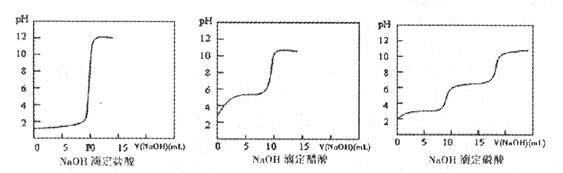
根据上述曲线回答下列问题:
①20℃时,三种酸从强到弱的顺序是;
②滴定开始后醋酸曲线变化比盐酸快的原因是;
③醋酸恰好中和时pH≈8的原因是;
④你认为前述的步骤中,NaOH滴定磷酸是否可行?(填“可行”、“不可行”)。