实验室有一瓶混有氯化钠的氢氧化钠固体试剂,经测定NaOH的质量分数约为82.0%,为了验证其纯度,用浓度为0.2 mol/L的盐酸进行滴定,试回答下列问题:
(1)托盘天平称量5.0 g固体试剂,用500 mL容量瓶中配成待测液备用。
(2)将标准盐酸装在已经润洗过的25.00 mL酸式滴定管中,调节液面位置在 处,并 记下刻度。
记下刻度。
(3)取20.00 mL待测液,待测定。用甲基橙试剂作指示剂时,滴定到溶液颜色由 刚好至 色时为止。
(4)滴定达终点后,记下盐酸用去20.00 mL,计算NaOH的质量分数为 。
(5)试分析滴定误差可能由下列哪 些实验
些实验 操作引起的 。
操作引起的 。
| A.转移待测液至容量瓶时,未洗涤烧杯 |
| B.酸式滴定管用蒸馏水洗涤后,直接装盐酸 |
| C.滴定时,反应容器摇动太激烈,有少量待测液溅出 |
| D.滴定到终点时,滴定管尖嘴悬有液滴 |
E.读滴定管开始时仰视,读终点时俯视
海水中可提取多种化工原料,下面是工业上对海水的几项综合利用示意图。
按要求回答问题:
(1)浩瀚的海洋是一个巨大的宝库,蕴含有80多种元素,可供提取利用的有50多种。下列物质不需要通过化学变化就能够从海水中获得的是。
A.食盐B.金属钠C.淡水
(2)以电解食盐水为基础制取Cl2、等产品的工业称为“氯碱工业”。
(3)实验室制取氯气的反应原理为:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O;根据上述实验原理,从下列装置中选择合适的发生装置用于实验室制取少量氯气(填写装置的序号)。
MnCl2+Cl2↑+2H2O;根据上述实验原理,从下列装置中选择合适的发生装置用于实验室制取少量氯气(填写装置的序号)。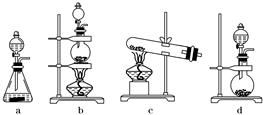
(4)实验室中模拟Br—→Br2的转化,可以通过在KBr溶液中滴加少量新制氯水的实验进行实现。写出Br—→Br2的转化离子方程式为:;氯水不稳定,要现用现配,下列吸收氯气制备氯水的装置最合理的是(选填下列选项的编号字母)。
(5)电解熔融氯化镁所得的镁蒸气冷却后即为固体镁。下列气体中,镁蒸气可以在其氛围中冷却的是 (选填下列选项的编号字母)。
A.Cl2 B.N2 C.Ar D.空气 E.H2
(1)甲同学在用FeSO4固体配制FeSO4溶液时,除了加入蒸馏水外,还需加和试剂(填化学式)
(2)乙同学为标定某醋酸溶液的准确浓度,用0.2000 mol·L—1的NaOH溶液对20.00mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下:
| 实验序号 |
1 |
2 |
3 |
4 |
| 消耗NaOH溶液的体积(mL) |
20.05 |
20.00 |
18.80 |
19.95 |
则该醋酸溶液的准确浓度为。(保留小数点后四位)
(3)丙同学利用:5Fe2++MnO4-+8H+===5Fe3++Mn2++4H2O反应,用KMnO4溶液滴定某样品进行铁元素含量的测定。
①设计的下列滴定方式,最合理的是_____。(夹持部分略去)(填字母序号)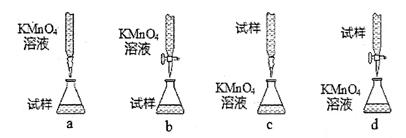
②判断滴定终点的依据是。
工业上常用铁质容器盛装冷浓硫酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是
另称取铁钉6.0g放入15.0ml浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。
(2)甲同学认为X中除Fe3+外还可能含有Fe2+,若要确认其中的Fe2+,可选用(选填序号)。
a.KSCN溶液和氯水b.K3Fe(CN)6溶液c.浓氨水d.酸性KMnO4溶液
由于Fe(OH)2极易被氧化,所以实验室难用亚铁盐
溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀.若用如图所
示实验装置可制得纯净的Fe(OH)2沉淀.两极材料分别为石
墨和铁。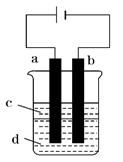
(1)a电极材料为,其电极反应式为。
(2)若电解液d是(填字母编号,下同),则白色沉淀在电极上生成;若是,则白色沉淀在两极之间的溶液中生成。
| A.纯水 | B.NaCl溶液 | C.NaOH溶液 | D.CuCl2溶液 |
(3)液体c为苯,其作用是,在加入苯之前,要对d溶液进行(填操作名称)处理,其目的是除去溶液中溶解的氧气。
(4)若装置中生成的气体在标准状况下的体积为2.24L,则生成的沉淀质量为g。
某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如下图所示: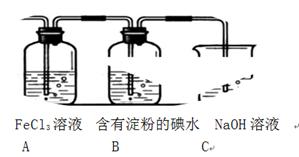
(1)SO2气体还原Fe3+的产物是(填离子符号),参加反应的SO2和Fe3+的物质的量之比是。
(2)下列实验方案适用于在实验室制取所需SO2的是(填序号)。
A.Na2SO3溶液与HNO3 B.Na2SO3固体与浓硫酸
C.固体硫在纯氧中燃烧D.硫铁矿在高温下与O2反应
(3)装置C的作用是。
(4)若要从A中所得溶液提取晶体,必须进行的实验操作步骤:蒸发、冷却结晶、过滤、自然干燥,在这一系列操作中没有用到的仪器有(填序号)。
A.蒸发皿 B.石棉网 C.漏斗 D.烧杯 E.玻璃棒 F.坩埚
(5)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入KMnO4溶液,紫红色褪去。
方案②:往第二份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
方案③:往第三份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案不合理的是,原因是。
(6)能表明I-的还原性弱于SO2的现象是。