已知:
(1)Cu2+、Fe2+在pH为4~5的条件下不水解,而这一条件下Fe3+几乎全部水解。
(2)双氧水(H2O2)是强氧化剂,在酸性条件下,它的还原产物是H2O。现用粗氧化铜(含少量Fe杂质)制取CuCl2溶液的过程如下:
①取50mL纯净的盐酸,加入一定量的粗CuO加热搅拌、充分反应后过滤,测知滤液的pH=3。②向滤液中加入双氧水、搅拌。
③调节②中溶液的pH至4,过滤。
④把③所得滤液浓缩得到CuCl2溶液。
回答下列问题:
(1)②中发生反应的离子方程是 。
(2)③中使pH升高到4,采取的措施是:加入过量的 (填字母序号)并微热、搅拌。
| A.NaOH | B.氨水 | C.CuCl2 | D.CuO |
(3)③中过滤后滤渣的成分是 。
长托宁是一种选择性抗胆碱药,可通过以下方法合成(部分反应条件略去):
(1)长托宁中的含氧官能团为_________和_________(填名称)
(2)反应②中加入试剂X的分子式为C8H6O3 ,X的结构简式为_________
(3)反应③的反应类型为_______________
(4)S的同分异构体满足下列条件:
①.能与FeCl3溶液发生显色反应。
②.核磁共振氢谱有5个峰且峰的面积比为2:4:4:1:1;分子中含有两个苯环。写出该同分异构体的结构简式_________________
(5)根据已有知识并结合相关信息,写出以 和
和 为原料制备
为原料制备 的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
实验室用辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)制备碱式碳酸铜的主要实验流程如下。
(1)滤渣Ⅰ的成分为MnO2、单质S和(写化学式);硫酸浸取时,Cu2S被MnO2氧化的化学方程式为。
(2)浸取时,Fe2O3溶于硫酸的离子方程式为;研究发现若先除铁再浸取,浸取速率明显变慢,其可能原因是。
(3)“赶氨”时,最适宜的操作方法是。
(4)滤液Ⅱ经蒸发结晶得到的盐主要是(写化学式)。
(4分)某温度下,在2 L密闭容器中,x、y、z三种物质的物质的量随时间变化曲线如图所示,
由图分析:
(1)该反应的化学方程式是_________________。
(2)3 min末,用y的浓度变化表示的反应速率V(y)为___________。
(3)反应是由_____________开始的反应。
A.正反应 B.逆反应 C.正、逆反应同时
在一定温度下,把2 mol N2和6 mol H2通入一个体积不变的密闭容器中,(如图)
容器中发生以下的反应:N2(g)+3H2(g)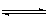 2NH3(g)(正反应为放热反应)若反应达到平衡后,测得混和气体为7mol,据此回答下列问题:保持上述反应温度不变,使a、b、c分别代表初始加入的N2、H2和NH3的物质的量,如果反应达到平衡后混和气体中各物质的物质的量分数仍与上述平衡时完全相同,那么:
2NH3(g)(正反应为放热反应)若反应达到平衡后,测得混和气体为7mol,据此回答下列问题:保持上述反应温度不变,使a、b、c分别代表初始加入的N2、H2和NH3的物质的量,如果反应达到平衡后混和气体中各物质的物质的量分数仍与上述平衡时完全相同,那么:
(1)若a="1" mol ,c="2" mol ,则b="____" mol,在此情况下,反应起始时将向方向进行(填“正”或“逆”)
(2)若规定起始时反应向逆反应方向进行,则c的范围是。
(3)在上述装置中,若需控制平衡后的混和气体的物质的量为6.5 mol,则可采取的措施是
某温度时,A+B 2C反应达到平衡状态,如果A为气体,且压强增大时,A的平衡浓度增大,则B为_________态或__________态,C为________态;如果减少或增加B的量,平衡不移动,则B是__________态;如果降温,C的平衡浓度降低,此反应的逆反应是___________热反应。
2C反应达到平衡状态,如果A为气体,且压强增大时,A的平衡浓度增大,则B为_________态或__________态,C为________态;如果减少或增加B的量,平衡不移动,则B是__________态;如果降温,C的平衡浓度降低,此反应的逆反应是___________热反应。