(1)SO2的摩尔质量为 ,1molSO2中含有氧原子的个数为 ,标况下5.6LSO2的质量为 。
(2)用20g烧碱配制成500mL溶液,其物质的量浓度为 mol/L;从中取出1mL,其物质的量浓度为 mol/L;若将这1mL溶液用水稀释到100mL,所得溶液中溶质的物质的量浓度为 mol/L。
一卤代烃RX与金属钠作用,可以增加碳链制取高级烃。反应的化学方程式为
RX+2Na+R′XR R′+2NaX其中X表示卤原子,R和R′表示为烃基,可以相同,也可以不同。试以苯、乙炔、Br2、HBr、Na为主要原料通过三步反应制取
R′+2NaX其中X表示卤原子,R和R′表示为烃基,可以相同,也可以不同。试以苯、乙炔、Br2、HBr、Na为主要原料通过三步反应制取 。其制取的化学方程式为:
。其制取的化学方程式为:
①__________________________________________________;
②__________________________________________________;
③__________________________________________________。
A、B、C、D四种有机物分子中的碳原子数目相同。标准状况下烃A对氢气的相对密度是13;烃B跟HBr反应生成C;C与D混合后加入NaOH并加热,可生成B。
(1)写出有机物的结构简式:A_________;D_________。
(2)写出有关反应的化学方程式:___________________________。
聚四氟乙烯的耐热性和化学稳定性都超过了其他合成材料,号称“塑料王”。在工业生产上有广泛的应用,其合成路线如下: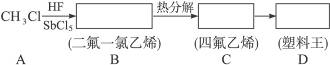
试完成下列各题:
(1)在直方框内填写有机物的结构简式。
(2)写出下列反应的化学方程式:
B→C:__________________________________________________________________;
C→D:__________________________________________________________________。
某一溴代烷A与氢氧化钠溶液混合后充分振荡,生成有机物B;A在氢氧化钠和B的混合液中共热生成一种气体C;C可由B与浓H2SO4混合加热制得,C可作果实催熟剂。则:
(1)A的结构简式为:______________________。
(2)A生成B的化学方程式:______________________。
(3)A生成C的化学方程式:______________________。
(4)B生成C的反应类型:______________________。
在NaCl溶液中滴入AgNO3溶液,现象为_____________________,离子方程式为_____________________。在CH3CH2Cl中滴加AgNO3溶液,现象为______________________,原因是______________________。若将CH3CH2Cl跟NaOH溶液共热,然后用稀HNO3酸化,再滴入AgNO3溶液,现象为______________,反应的化学方程式为______________________。