A、B、C、D是中学化学的常见物质,其中A、B、C均含有同一种元素。在一定条件下相互转化的关系如下图所示(部分反应中的H2O已略去)。请填空: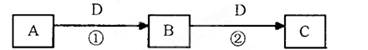
(1)若A可用于自来水消毒,D是生产、生活中用量大、用途广的金属单质,写出C转化为B的化学方程式为 ;用A制漂白粉的反应方程式为 。
(2)若D与C60互为同素异形体,A与O3互为同素异形体,则C在高炉炼铁中的主要反应方程式为 。
(3)若D是空气质量预报要报的气体,相同条件下密度是氧气的两倍,A是烧碱溶液,则可以验证B是否变质的一组试剂是 (请写出试剂名称)。若已部分变质则实验现象为 。
(4)若A、B、C均为两种元素组成的非电解质且常温下均为气态,则反应①的化学方程式为 。
下表为元素周期表的一部分,参照元素①~⑨在表中的位置,按要求回答下列问题: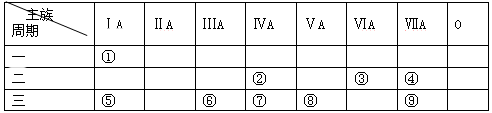
(1)在标号元素中,最活泼的金属元素名称是最活泼的非金属元素名称是。
⑨元素的原子结构简示意图(2分)。
(2)用电子式表示 ①与②形成共价化合物的形成过程(2分)。
(3)⑤、⑥、⑦三种元素的原子半径由大到小的顺序是(序号表示,2分)。
(4)①~⑨元素所形成的气态氢化物中,最稳定的是(化学式表示,2分)
⑦、⑧、⑨三种元素的气态氢化物的稳定由强到弱的顺序 (化学式表示,2分)。
(5)写出元素⑨的单质与溴化钠反应的离子方程式:(2分)。
A、B、C、D四种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,D的L层电子数等于K、M两个电子层上的电子数之和。
(1)A为,B为,C为,D为。(填写相应的元素符号)
(2)写出A、B的化合物与E反应的化学方程式:。
(3)C元素的最高价氧化物的水化物与铝的氧化物对应的水化物反应的方程式 。
(4)写出D元素的最高价氧化物的水化物浓溶液和A反应的化学方程式:。
填空题 (每空2分,共 18 分)
(1)回答下列变化是哪些能量形式间的转化:
A用蓄电池点亮灯泡B植物的光合作用,C高温分解碳酸钙
(2)书写下列物质电子式 Na2O2
(3)用电子式表示下列物质的形成过程
CaCl2
(4)根据同主族元素性质的相似性和递变性进行预测:(各2分)
①酸性强弱:H3AsO4 H3PO4(用“>”或“<”表示,下同)
②沸点:HFHCl
(5)推测原子序数为34的元素硒(Se)处于元素周期表中族,关于Se的预测正确的是
| A.常温下Se单质是气体 |
| B.Se最高价氧化物的水化物能和NaOH发生反应 |
| C.氢化物的化学式为H2Se |
| D.常见的氧化物只有SeO3 |
某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图。加热聚丙烯废塑料得到的产物如下表:
| 产物 |
氢气 |
甲烷 |
乙烯 |
丙烯 |
苯 |
甲苯 |
碳 |
| 质量分数(%) |
12 |
24 |
12 |
16 |
20 |
10 |
6 |
(1)试管A中残余物有多种用途,如下列转化就可制取高聚物聚乙炔。
A中残留物 电石
电石 乙炔
乙炔 聚乙炔
聚乙炔
写出反应②和③的化学方程式:②______________________________;
③______________________________;
(2)试管B收集到的产品中,能使酸性高锰酸钾溶液褪色的物质,其一氯代物的结构简式分别是
______________________________________________________。
(3)锥形瓶C中观察到的现象:______________________________。
(4)写出C中逸出的气体在工业上的两种用途__________、__________。
已知某种燃料含有碳、氢、氧三种元素。为了测定这种燃料中碳和氢两种元素的质量比,可将气态燃料放入足量的O2中燃烧,并将产生的气体全部通过图示装置,得到如表所列的实验数据(产生的气体完全被吸收)。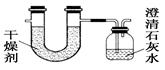
| 实验前 |
实验后 |
|
| (干燥剂+U形管)的质量 |
101.1g |
102.9g |
| (澄清石灰水+广口瓶)的质量 |
312.0g |
314.2g |
根据实验数据填空:
(1)实验完毕后,生成物中水的质量为____g,假设广口瓶里生成一种正盐,其质量为______g。
(2)生成的水中氢元素的质量为________g。
(3)生成的CO2中碳元素的质量为________g。
(4)该燃料中碳、氢元素质量比为________.