(12分)实验室制取Cl2及性质的验证实验组合装置如下:
A B C D E F G
回答下列问题:
(1)A中的化学方程式为 。
(2)B的作用是除去HCl气体,C的作用是 。
(3)E、F中观察到的现象分别是 ,你得到的结论是 。
(4)G的作用是 ,
化学方程式为 。
(12分)Ⅰ.从下列各组反应对比,判断哪种微粒的氧化性最强。
(1)在氯气中Fe锈蚀成棕褐色物质FeCl3,而在盐酸中生成淡绿色溶液FeCl2。则氯气分子、氢离子、氯离子中,__________具有氧化性,__________氧化性最强。请书写出以上各反应的化学方程式___________________________。
(2)已知在ⅣA族元素中,Pb2+和Sn4+的化合物较为稳定。
据此可判断PbO2具有较强的________性,SnCl2具有较强的________性;写出PbO2溶于盐酸的离子方程式____________________;写出SnCl2和FeCl3溶液混合的离子方程式_______________________________________
Ⅱ.氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40°C~50°C时反应可生成它。CuH具有的性质有:不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成气体;Cu+在酸性条件下发生的反应是:2Cu+===Cu2++Cu。
根据以上信息,结合自己所掌握的化学知识,回答下列问题:
(1)用CuSO4溶液和“另一物质”制CuH的反应中,用氧化还原观点分析,这“另一物质”在反应中作________(填“氧化剂”或“还原剂”)。
(2)写出CuH在氯气中燃烧的化学反应方程式:________________。
(3)CuH溶解在稀盐酸中生成的气体是____________(填化学式)。
(4)如果把CuH溶解在足量的稀硝酸中生成的气体只有NO,请写出CuH溶解在足量稀硝酸中反应的离子方程式: ______________________________。
一包白色粉末可能含有Ba(NO3)2、C uSO4、K2CO3、NaCl、Na2SO4、K
uSO4、K2CO3、NaCl、Na2SO4、K NO3中的一种或几种,为判断其组成,进行如下实验:①取少量该白色粉末溶于水,产生白色沉淀,上层清液为无色;②取上层清液滴在pH试纸上,pH>7;③过滤,往得到的白色沉淀中滴入稀盐酸,白色沉淀部分溶解。则该白色粉末中一定含有_____________________,一定没有_________,可能含有________________________。
NO3中的一种或几种,为判断其组成,进行如下实验:①取少量该白色粉末溶于水,产生白色沉淀,上层清液为无色;②取上层清液滴在pH试纸上,pH>7;③过滤,往得到的白色沉淀中滴入稀盐酸,白色沉淀部分溶解。则该白色粉末中一定含有_____________________,一定没有_________,可能含有________________________。
按要求写出下列反应的化学方程 式;
式;
①将硫酸氢钠与氢氧化钡在溶液中按物质的量之比2︰1混合,则离子方程式:___________________________________。
②将硫酸氢钠与氢氧化钡在溶液中按物质的量之比1︰1混合,则化学方程式:____________________________________
③实验室用金属铜和浓硝酸制取二氧化氮的化学方程式:___________.
④氨的催化氧化:______________________________________.
在两份体积相同的NaOH溶液中,分别通入CO2气体,充分反应后,在所得溶液A、B中分别加入1mol/L的盐酸,所加盐酸体积(mL)与产生CO2气体的体积(L)的关系如图所示,试填写下列空白:
⑴两份NaOH溶液A和B的物质的量浓度之比为,通入CO2气体的体积之比是(相同条件)。
⑵与盐酸反应前,A溶液中的溶质是,其物质的量之比是。
⑶与盐酸反应前,B溶液中的溶质是,其物质的量之比是。
在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物。该氧化物又可以经过此反应的逆反应,生成颗粒很细的铁粉。这种铁粉具有很高的反应活性,在空气中受撞击或受热时会燃烧,所以俗称“引火铁”。请分别用图中示意的两套仪器装置,制取上述铁的氧化物(左)和“引火铁”(右)。实验中必须使用普通铁粉和6mol/L盐酸,其他试剂自选(装置中必要的铁架台、铁夹、铁圈、石棉网、加热 设备等在图中均已略去)。
设备等在图中均已略去)。
填写下列空白:
⑴实验进行时试管A中应加入的试剂是______;
烧瓶B的作用是____________________;
在试管D中收集得到的是_______________。
⑵实验时,U型管G中应加入的试剂是____________;
长颈漏斗H中应加入___________。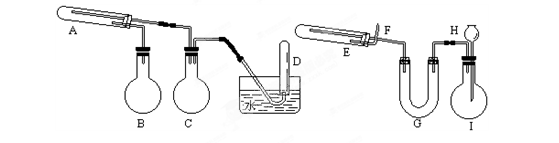 ⑶两套装置中,在实验时需要加热的仪器是(填该仪器对应的字母)__________。
⑶两套装置中,在实验时需要加热的仪器是(填该仪器对应的字母)__________。
⑷试管E中发生反应的化学方程式是_______________。
⑸为了安全,在E管中的反应发生前,在F 出口处必须_____________________。
出口处必须_____________________。