(每空2分,共12分)化学课后,化学兴趣小组的同学在整理实验桌时,发现有一瓶氢氧化钠溶液没有塞橡皮塞,征得老师同意后,开展了以下探究:
[提出问题1] 该氢氧化钠溶液是否变质了呢?
[实验探究1]
| 实验操作 |
实验现象 |
实验结论 |
| 取少量该溶液于试管中,向溶液中滴加稀盐酸,并不断振荡。 |
有气泡冒出。 |
氢氧化钠溶液一定变质了。 |
[提出问题2] 该氢氧化钠溶液是全部变质还是部分变质呢?
[猜想与假设]
猜想1:氢氧化钠溶液部分变质。
猜想2:氢氧化钠溶液全部变质。
[查阅资料] (1)氯化钙溶液呈中性。
(2)氯化钙溶液能与碳酸钠溶液反应:CaCl2+Na2CO3=CaCO3↓+2NaCl
[实验探究2]
| 实验步骤 |
实验现象 |
实验结论 |
| (1)取少量该溶液于试管中,向溶液中滴加过量的氯化钙溶液,并不断振荡。 |
有 生成。 |
明原溶液中一定有碳酸钠。 |
(2)取步骤(1)试管中的少 量上层清液,滴加酚酞溶液。 量上层清液,滴加酚酞溶液。 |
溶液变红色。 |
说明原溶液中一定有 。 |
[实验结论] 该氢氧化钠溶液 (填“部分”或“全部”)变质。
[反思与评价] (1)氢氧化钠溶液露置于空气中容易变质,请写出相关反应的化学方程式: 。
(2)在上述[实验探究2]中,小明提出可用氢氧化钙溶液代替氯化钙溶液,你认为该方案
(填“可行”或“不可行”)。
[理解与应用]氢氧化钠溶液容易变质,必须密封保存。实验室必须密封保存的药品还有很多,试另举一例:
在实验研究中,同学们对某品牌牙膏中的摩擦剂成分及其含量进行测定。
【查阅资料】
①该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸时无气体产生。
②饱和碳酸氢钠溶液不吸收二氧化碳气体;
③碳酸氢钠可与盐酸反应:NaHCO3+HCl→NaCl+H2O+CO2↑
根据以上资料,设计下列实验:
【实验分析】用下图所示装置测定牙膏样品中碳酸钙的含量。
①装置A中氢氧化钠溶液的作用是(32)。
②C中观察到有沉淀产生,反应的化学方程式为 (33)。
③实验过程中需持续缓缓通入空气,其作用:(34)。
④装置D中碱石灰用于吸收空气中的二氧化碳和水蒸气,其中氧化钙吸收水反应的化学方程式为(35)。
【解释与结论】实验测得如下数据:
| 实验次数 |
样品质量(g) |
所用盐酸质量(g) |
所得沉淀质量(g) |
| 第一次 |
6.8 |
40.0 |
1.62 |
| 第二次 |
6.8 |
40.0 |
1.66 |
| 第三次 |
6.8 |
40.0 |
1.65 |
欲计算样品中碳酸钙的含量,应选择的数据是(36)。
【反思与评价】
①有人认为不必测定C中沉淀的质量,只要测定装置C在吸收CO2前后的质量差,同样可以确定碳酸钙的质量分数。实验证明按此方法测定的结果偏高,原因可能是(37)。
②有同学设计出提高测定准确度的方法。下列各项措施中,不合理的是(38)(填序号)。
Ⅰ.在加入盐酸之前,排净装置内含有的CO2气体
Ⅱ.把盐酸换成稀硫酸
Ⅲ.在B-C之间增添盛有饱和碳酸氢钠溶液的洗气装置
硝酸铜为蓝色固体,溶于水可得蓝色溶液。某实验小组同学用下图装置加热硝酸铜,发现固体由蓝色逐渐变黑,同时产生红棕色有刺激性气味的气体,带火星的木条复燃。
【提出问题】硝酸铜在加热条件下到底发生了怎样的反应?
【查阅资料】
①氧化铜和稀硫酸反应的化学方程式:CuO+H2SO4 CuSO4+H2O
CuSO4+H2O
②含氮化合物中,只有NO2是红棕色、有刺激性气味的气体。
③NO2有助燃性,能使带火星的木条复燃
【猜想假设】
Cu(NO3)2受热分解除了生成_______,还可能生成了CuO和O2。
【进行实验】
| 实验操作 |
实验现象 |
实验结论 |
| 步骤I:将反应后试管中的固体加水充分溶解, ①,加热 |
固体全部溶解,得到蓝色溶液 |
硝酸铜分解生成了氧化铜。 |
步骤II:在图1的试管和集气瓶之间连上如图所示的装置,重新进行加热硝酸铜的实验 |
集气瓶中气体为无色,带火星木条复燃 |
硝酸铜分解生成了氧气 |
步骤II是同学们查阅了新的资料后设计完成的。该资料是关于NO2___②__方面的性质信息。
【获得结论】根据实验结果,Cu(NO3)2受热分解的化学方程式为_______。
【反思与评价】已知相同状况下,气体的体积比等于其分子个数比。据此,同学们认为,即使没有资料③,依据实验结论和“加热硝酸铜产生的气体能使带火星的木条复燃”的实验现象,也能推出NO2可能具有助燃性。理由是______。
结合教材中关于二氧化碳收集方法的描述:二氧化碳能溶于水,一般不用排水法收集。某化学小组分成两组进行实验,研究是否能用排水法收集二氧化碳的问题。
[查阅资料]二氧化碳不溶于饱和碳酸氢钠溶液。
[知识储备]写出下列化学方程式:
①实验室制备二氧化碳的反应。
②二氧化碳与水反应。
(1)实验一:
步骤一:室温下,取大小相同的两个集气瓶,用向上排空气法收集两瓶二氧化碳气体,小心地由瓶壁向瓶中各加入半瓶蒸馏水,瓶1用玻璃片盖好,瓶2盖上胶塞迅速振荡后,取下胶塞盖好玻璃片,两瓶静置相同的时间。
步骤二用燃着的木条同时伸入两瓶,观察到瓶1中的木条熄灭比瓶2中的快。
[实验结论]该实验说明,二氧化碳溶于水的量的多少与(填字母序号)有关。
| A.水量的多少 | B.水的温度 |
| C.气体与水的接触面积 | D.气体与水的接触时间 |
[实验二]
室温下,用图1所示装置向试管内长时间通入二氧化碳;用图2所示装置,收集一瓶二氧化碳。用pH计测得室温下三种液体的pH,记入下表。
| 液体 |
所用蒸馏水 |
试管内 |
烧杯内 |
| pH |
a1 |
a2 |
a3=6.94 |
[实验结论]
由a3数据可知,用图2所示装置收集二氧化碳时,二氧化碳在水中溶解的量很小。
根据上述结论,推测a1、a2和a3由小到大的顺序是。
[反思与交流]饱和碳酸氢钠溶液的作用是。
[实验结论]用图2所示装置,可以收集二氧化碳。
某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格).
【演示实验】将一定量的稀H2SO4加入到盛有KOH溶液的小烧杯中.
【学生板演】该反应的化学方程式(23).
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
【假设猜想】针对疑问,太家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有K2SO4
猜想二:有K2SO4和H2SO4
猜想三:有K2SO4和KOH
猜想四:有K2SO4、H2SO4和KOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是(24).
【实验探究】(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有(25).
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaC12溶液、Na2CO3溶液,进行如下三个方案的探究.
| 实验方案 |
测溶液pH |
滴加Na2CO3溶液 |
滴加BaCl2溶液 |
| 实验操作 |
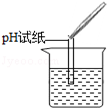 |
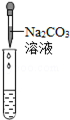 |
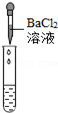 |
| 实验现象 |
试纸变色,对比比色卡,pH<7 |
有气泡产生 |
产生白色沉淀 |
| 实验结论 |
溶液中有H2SO4 |
溶液中有H2SO4 |
溶液中有H2SO4 |
【得出结论】通过探究,全班同学一致确定______(26)__________是正确的.
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出
【实验探究】(2)中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:
(1)实验操作中的错误是(27).
(2)实验方案中也有一个是错误的,错误的原因是(28)
某同学对三种牙膏的成分和性质进行如下探究。
①测定牙膏的pH。
甲:pH=8.5乙:pH=7.0丙:pH=6.5能缓解牙齿酸痛的碱性牙膏是( 33)(填“甲”、“乙”、“丙”)。
②检验牙膏中是否含有碳酸钙。
该同学用检验碳酸盐的方法检验牙膏中是否含有碳酸钙,实验记录如下。
| 实验步骤 |
实验现象 |
实验结论 |
| 各取三种牙膏膏体于试管中,加入适量稀盐酸。 |
甲、乙牙膏的表面( 34);丙牙膏的表面无明显现象。 |
甲、乙牙膏中含碳酸钙,丙牙膏中不含碳酸钙。 |
上述实验不够完善,还需增加的一步操作是( 35) 。
③比较甲、乙牙膏中碳酸钙的质量分数。
【实验原理】通过测定逸出气体的质量,可计算出碳酸钙的质量分数(牙膏中其它物质不与盐酸反应)。
【实验步骤】按下图装置进行实验,记录不同时刻装置和药品的总质量,数据如下: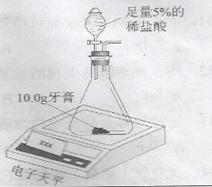
| 时间(min) |
0 |
2 |
4 |
6 |
8 |
10 |
12 |
|
| 装置和药品总质量(g) |
牙膏甲 |
261.0 |
260.0 |
259.3 |
258.8 |
258.5[ |
258.5 |
258.5 |
| 牙膏乙 |
263.0 |
262.4 |
261.9 |
261.4 |
261.0 |
261.0 |
261.0 |
【实验结论】( 36);
【实验反思】经查实,上述方法所测得的两种牙膏的碳酸钙含量均偏小(实验操作规范),导致偏小的原因可能是( 37) 。
A.盐酸挥发B.有水蒸气逸出
C.装置漏气 D.锥形瓶内残留二氧化碳