(16分)化学兴趣小组对某品牌牙膏中摩擦剂成分及其含量进行以下探究:
查得资料:该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸时无气体生成。
I、摩擦剂中氢氧化铝的定性检验
取适量牙膏样品,加水搅拌、过滤。并进行如下实验
(1)、请完成表格中的填空:
| 实验步骤 |
实现现象 |
反应的离子方程式 |
| 往滤渣中加入过量NaOH溶液。 |
|
① |
| 过滤,往所得滤液中通入过量二氧化碳, |
② |
③ |
| 继续加入过量稀盐酸 |
④ |
|
II、牙膏样品中碳酸钙的定量测定
利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数。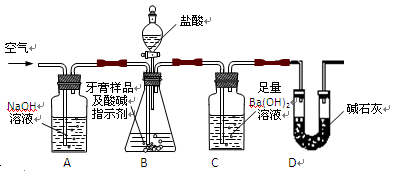
依据实验过程回答下列问题:
(2)、实验过程中先后两次鼓入空气,第二次鼓入空气的目的是:
。
(3)、C中反应生成BaCO3的化学方程式是 。
(4)、下列各项措施中,不能提高测定准确度的是 (填标号)。
A.在加入盐酸之前,应排净装置内的CO2气体
B.滴加盐酸不宜过快
C.在A—B之间增添盛有浓硫酸的洗气装置
D.在B—C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(5)、实验中准确称取8.00g样品三份,进行三次测定,测得BaCO3平均质量为3.94g.则样品中碳酸钙的质量分数为 。
(6)、某同学提出将C中的Ba(OH)2换成浓H2SO4,通过测定D装置反应前后的质量差也可以测定CaCO3的含量,假设反应前D装置的质量为m1,实验结束后D装置的质量为m2,则样品中CaCO3的质量为 。实验证明按此测定的结果偏高,原因是 。
某化学兴趣小组按照下列方案进行“由含铁废铝制备硫酸铝晶体”的实验:
步骤1:取一定量含铁废铝,加足量的NaOH溶液,反应完全后过滤。
步骤2:边搅拌边向溶液中滴加稀硫酸至溶液pH=8~9,静置、过滤、洗涤。
步骤3:将步骤2中得到的固体溶于足量的稀硫酸。
步骤4:将得到的溶液范发浓缩、冷却、结晶、过滤、干燥。
请回答以下问题:
(1)上述实验中的过滤操作需要玻璃棒、_______、_______等玻璃仪器。
(2)步骤1过滤的目的是______________。
(3)当步骤2中溶液的pH=8~9时,检验沉淀是否完全的方法是______________。
(4)步骤2中溶液的pH较难控制,可改用_______。
著名化学家罗伯特·波义耳(RobertBoyle)在一次实验中,不小心将盐酸溅到紫罗兰花瓣上,过了一会儿,他惊奇地发现,紫色的花瓣上出现了红点。波义耳对这一意外的发现作出了多种假设,经过多次实验验证,探究普遍规律,终于获得了成功。对紫罗兰花瓣遇盐酸变红的现象,你有哪些假设?请将你的各种假设以及验证假设的实验方案填写在下表中。
| 你对紫罗兰花瓣遇盐酸变红现象的各种假设 |
你验证假设的实验方案 |
为探究淀粉的水解,某同学设计了下列实验:
银氨溶液,温水浴 现象A

 淀粉
淀粉  水解液
水解液  中和液
中和液 碘溶液现象B
碘溶液现象B
⑴取少量反应液,用碱中和硫酸,加入银氨溶液,水浴加热,如果现象A是出现光亮的银镜,说明淀粉 (填“已水解”或“未水解”),反应的化学方程式为
⑵另取少量反应液,加入少量碘溶液,观察是否有颜色变化,如果无明显现象,证明淀粉已经 ,如果溶液出现蓝色,证明淀粉 (填“部分水解”或“完全水解”)
 |
某课外活动小组利用如图所示装置分别做如下实验: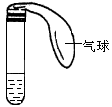
①在试管中注入某红色溶液,加热试管,溶液颜色变浅,冷却后
恢复红色,则原溶液可能是________________溶液;加热时溶液由红色逐渐变浅的原因是:_________________________。②在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复无色,则此溶液可能是_____________溶液;加热时溶液由无色变为红色的原因是:__________________________________。
在学习“塑料、橡胶和纤维”时,我们对几种纤维的性质进行了科学探究。
①取一小块纯棉布、羊毛织物(或蚕丝织物)和尼龙布,分别在酒精灯火焰上灼烧,观察现象。②另取上述材料各一小块,分别浸入10%H2SO4溶液和3%NaOH溶液中,微热5~6min,取出用水漂洗、烘干。③把通过②处理过的织物与没有用酸、碱处理的织物进行对比。
回答下列问题:⑴完成实验现象记录表。
| 灼烧情况 |
受10%H2SO4溶液影响情况 |
受3%NaOH溶液影响请况 |
|
| 纯棉布 |
易燃烧,有烧纸的气味,灰烬一触即碎 |
轻微 |
轻微 |
| 羊毛(或蚕丝织物) |
接近火焰卷缩,有味,灰烬为黑色、膨胀易碎的颗粒 |
||
| 尼龙布 |
接近火焰卷缩,有特殊气味,趁热可拉成丝,灰烬为灰褐色玻璃球状 |
几乎不变 |
几乎不变 |
⑵通过本次探究,你认为合成纤维(如尼龙)与天然纤维相比较,其突出性能是;
⑶对于纯棉布、羊毛(或蚕丝)和尼龙布衣物,你认为可以在较高温度下熨烫的是;
⑷加酶洗衣粉中的碱性蛋白酶制剂可以使奶渍、血渍等多种蛋白质污垢降解成易溶于水的小分子肽。在洗涤纯棉布、羊毛(或蚕丝)和尼龙布衣物时,你认为不能使用加酶洗衣粉的是。