下图是部分短周期元素的单质及其化合物(或其溶液)的转化关系,已知B、C、D、E是非金属单质,且在常温常压下都是气体,化合物G的焰色反应为黄色,化合物I和J通常状况下呈气态;反应①是化工生产中的一种重要固氮反应。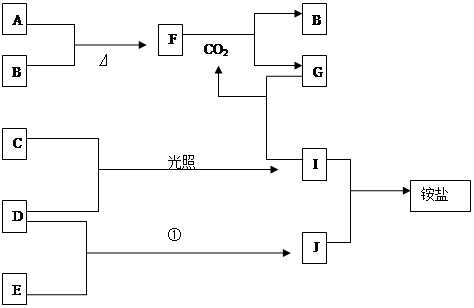
请回答下列问题:
(1)写出下列物质化学式:A B C
(2)写出下列物质间反应的化学方程式
A+B
F+CO2
D+E
I+J
(3)写出下列反应的离子方程式
G+I
(7分)盐酸、硫酸和硝酸是中学阶段常见的“三大酸”。现就三大酸与金属铜反应的情况,回答下列问题:
(1)稀盐酸不与Cu反应,若在稀盐酸中加入H2O2(常见氧化剂,作氧化剂时还原产物为水)后,则可使铜顺利溶解。该反应的化学方程式为:__________________________________。
(2)在一定体积的18 mol·L-1的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9mol。则浓硫酸的实际体积_________(填“大于”、“等于”或“小于”)100mL。若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为______________。
(3)根据下图操作及现象推断酸X为_______(填序号)。
a.浓盐酸 b.浓硫酸c.浓硝酸
用相关的化学用语表示下列物质:
⑴ 写出电子式Al3+Cl
⑵ 写出下列物质的结构式:N2 CO2
⑶ 用电子式表示NaOH_______________________
【化学—选修5:有机化学基础】
已知有机物A~I之间的转化关系如下图所示:
已知:
①A与D、B与E、I与F互为同分异构体
②将新制Cu(OH)2悬浊液分别加入到有机物I、F中,加热,I无明显现象,F反应并生成砖红色物质
③C的实验式与乙炔相同,且相对分子质量为104
④E的一种同分异构体与FeCl3能发生显色反应
根据以上信息,回答下列问题:
(1)H、 F中含有的含氧官能团名称分别为、。
(2)反应①~⑨中属于消去反应的是____________________________。
(3)I的结构简式为____________________________。
(4)写出H在酸性条件下水解的化学方程式。
(5)写出F与银氨溶液反应的化学方程式。
(6)符合以下条件的G的同分异构体有________种;其中苯环上只有2种一元取代物的结构简式为。
①属于芳香族化合物
②能与NaOH溶液反应
③能发生银镜反应
【化学—选修3:物质结构与性质】
a、b、c、d、f五种前四周期元素,原子序数依次增大;a、b、c三种元素的基态原子具有相同的能层和能级,第一电离能I1(a)<I1(c)<I1(b),且其中基态b原子的2p轨道处于半充满状态; d为周期表前四周期中电负性最小的元素;f的原子序数为29。请回答下列问题。(如需表示具体元素请用相应的元素符号)
(1)写出ac2的电子式__________;基态f原子的外围电子排布式为。
(2)写出一种与ac2互为等电子体的物质的化学式。
(3)b的简单氢化物的沸点比同族元素氢化物的沸点。(填“高”或“低”)
(4)化合物M由c、d两种元素组成,其晶胞结构如甲,则M的化学式为。
(5)化合物N的部分结构如乙,N由a、b两元素组成,则硬度超过金刚石。试回答:①N的晶体类型为________________________,其硬度超过金刚石的原因是___________________。
②N晶体中a、b两元素原子的杂化方式均为___________________。
【化学——选修2:化学与技术】
(一)硫酸厂常用煅烧黄铁矿(FeS2)来制取硫酸。
(1)煅烧黄铁矿的主要化学方程式为 。
(2)SO2和O2的反应为 2SO2(g)+O2(g) 2SO3(g),该反应在体积不变的密闭容器中进行,则下列(填序号)可作为反应达到平衡的判断依据。
2SO3(g),该反应在体积不变的密闭容器中进行,则下列(填序号)可作为反应达到平衡的判断依据。
A.v正(SO2)=v正(SO3)
B.各组分的体积分数不再变化
C.反应体系的温度不再变化
D.混合气体的平均相对分子质量不再变化
E.混合气体的密度不再变化
(3)热交换器是实现冷热交换的装置,化学实验中也经常利用热交换来实现某种实验目的。试分析气、液热交换时通常使用的仪器是________________________。(写名称)
(4)硫酸工业所产生的尾气除了含有N2、O2外,还含有SO2,微量的SO3和酸雾。能用于测定硫酸尾气中SO2含量的试剂是___________________。(填序号)
A.NaOH溶液、酚酞试液 B.KMnO4溶液、稀硫酸
C. 氨水、酚酞试液 D.碘水、淀粉溶液
(二)实验室常用硫酸厂的烧渣(主要成分是Fe2O3及少量FeS、SiO2)来制备绿矾(FeSO4·7H2O)。
其中测定绿矾产品中FeSO4·7H2O含量的实验步骤为:
a.称取5.2 g产品,溶解,配成250 mL溶液
b.量取25.00 ml待测液于锥形瓶中
c.用硫酸酸化的0. 01 mol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积35.00 mL。
据此,请分析:
(1)滴定时反应的离子方程式为(完成并配平离子反应方程式)。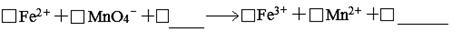
(2)滴定达到终点的标志是。
(3)产品中FeSO4·7H2O的质量分数为。