氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,附气体的能力强,性质稳定,请回答: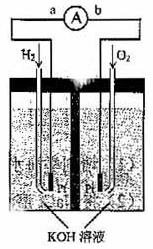
(1)氢氧燃料电池的能量转化主要形式是 ,在导线中电子流动方向为
(用a、b表示) 。(2)负极反应式为 。
(3)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一,金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
Ⅰ.2Li+H2 2LiH
2LiH
Ⅱ.LiH+H2O==LiOH+H2↑
①反应Ⅰ中的还原剂是 ,反应Ⅱ中的氧化剂是 。
②已知LiH固体密度为 0.82g/cm3。用锂吸收 224L(标准状况)H2,生成的LiH体积与被吸收的H2体积比为 。
③由②生成的LiH与H2O作用放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为 。
下列反应中,属于吸热反应的是。
①煅烧石灰石(主要成分是CaCO3)制生石灰(CaO)②燃烧木炭取暖③炸药爆炸 ④ 酸与碱的中和反应 ⑤ 生石灰与水作用制熟石灰 ⑥ 食物因氧化而腐败
从能量的角度看,断开化学键要,形成化学键要。一个化学反应是释放能量还是吸收能量取决于。
写出下列物质的电子式:①KCl;②Cl2;③H2O。
短周期元素中,A元素原子最外层电子数是次外层电子数的2倍;B元素的最高正价是+6价;C元素原子M层电子数等于其L层电子数的一半;D元素原子最外层有1个电子,D的阳离子与氖原子的电子层结构相同,则
(1)A:B:C:D:(填元素符号)
(2)B元素与氢元素形成的化合物所含化学键为(填 “共价键”或“离子键”)
下表是元素周期表的一部分, 针对表中的①~⑧种元素,填写下列空白:
| 主族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0族 |
| 2 |
① |
② |
③ |
|||||
| 3 |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
(1)元素⑥名称为在周期表中位于第周期,第族,元素⑧的原子结构示意图是。
(2)⑥、⑦氢化物的稳定性> (填化学式)。
(3)①、②、③三种元素按原子半径由小到大的顺序依次为(填元素符号)。
(4)在最高价氧化物的水化物中,酸性最强的化合物的分子式是;碱性最强的化合物的是_____________,该化合物属于(填 “共价”或“离子”)化合物。
(5)④元素与⑦元素形成的化合物的电子式是,高温下灼烧该化合物时,火焰呈色。
(6)元素⑤的单质与稀硫酸的反应是(填“放热”或“吸热”)反应。