已知由短周期常见元素形成的纯净物A、B、C、D、E、F、X转化关系如下图所示,B、X为单质,D常温下为无色液体,A、B含同一种元素。(某些产物可能略去)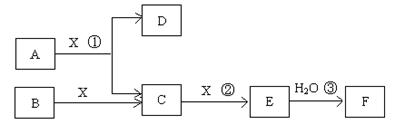
请回答下列问题:
(1)若E是有色气体,F是一元强酸,反应①是工业制备F的第一步反应。
①写出A与X反应的化学方程式: 。
②有人认为“浓H2SO4可以干燥气体E”。某同学为了验证该观点是否正确,用下图装置进行实验。实验过程中,浓H2SO4中未发现有气体逸出,且浓H2SO4由无色变为红棕色,由此你得出的结论是 。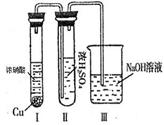
③已知常温下1 mol气体E发生反应③放出46kJ热量,写出气体E与H2O反应的热化学方式 。
④在常温下,向V1L pH=a的A溶液中加入V2L pH=b的盐酸,且a+b=14,若反应后溶液的pH<7,则V1和V2的关系为V1 V2(填>、<、无法确定),所得溶液中各种离子的浓度由大到小的顺序可能是 。(写出一种情况即可)
(2)若E为无色无味气体,F是二元弱酸。
①E的电子式为 ;
②将少量气体E通入氢氧化钡溶液中得不溶物G,G的KSP=8.1×10-9。现将该沉淀放入0.1mol/L的BaCl2溶液中,其KSP ,(填:增大、减小或不变),此时,组成不溶物G的阴离子在溶液中的浓度为 mol/L。
(4分)根据下列4组物质的结构简式回答:
① CH4和CH3CH3② CH2=CHCH3和CH3CH=CH2
③ CH3CH2CH2CH3和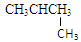 ④C2H5OH和CH3OCH3
④C2H5OH和CH3OCH3
(1)属于同系物的是。(2)属于同一物质的是。
(3)具有不同官能团的同分异构体是。
(4)由于碳链骨架不同而产生的同分异构体是。
某生活污水有一股臭味,主要含有碎菜叶、碎塑料薄膜、泥沙、氯化钠和碳酸钠等物质。现欲将其经去渣、除臭处理后用作清洗厕所的用水,问:
(1)采用何种操作,可除去污水中的碎菜叶,碎塑料薄膜及泥沙?
(2)用什么物质可除去污水中的臭味?(答对一种即可)
(3)把生活污水进行处理再利用的目的是什么?
(4)怎样检验(1)和(2)处理后的水中是否存在氯离子?
下表是某食品包装袋上的说明,从表中的配料中分别选出一种物质填在相应的横线上。
| 品名 |
××× |
| 配料 |
鲜鸡蛋、精面粉、白砂糖、精炼植物油、奶油、奶粉、碳酸氢钠、柠檬酸、柠檬汁、食盐、甜蜜素、菠萝香精、柠檬黄、日落黄、山梨酸钾等 |
| 保质期 |
240天 |
| 生产日期 |
标于包装袋封口上 |
(1)富含蛋白质的是___________________ 。
(2)富含糖类的是_____________________ 。
(3)富含油脂的是_____________________ 。
(4)富含维生素的是。
(5)属于着色剂的有。
(6)属于调味剂的有 [。
(7)属于防腐剂的有。
(8)属于疏松剂的有。
下表是元素周期表的一部分,列出了七种元素的周期表中的位置:
| ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
| 2 |
① |
② |
③ |
||||
| 3 |
④ |
⑤ |
⑥ |
⑦ |
请用化学符号按要求回答下列问题:
(1)这七种元素中,非金属性最强的是,在元素周期表中的位置
(2)元素①与②形成摩尔质量为44g /mol的物质,它的电子式是
(3)③、⑥、⑦三种元素的原子半径由大到小的顺序是。
(4)④元素最高价氧化物对应的水化物与⑥元素的最高价氧化物对应的水化物反应的化学反应方程式是
(5)④、⑤、⑥三种元素最高价氧化物的水化物碱性强弱顺序是
Q、R、X、Y、Z五种元素的原子序数依次递增。已知:
①Z的原子序数为29,其余的均为短周期主族元素;
②Y原子价电子(外围电子)排布为msnmpn;
③R原子核外L层电子数为奇数;
④Q、X原子p轨道的电子数分别为2和4。请回答下列问题:
(1)在[Z(NH3)4]2+离子中,Z2+的空轨道接受NH3分子提供的________形成配位键。
(2)Q与Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是________。
a.稳定性:甲>乙,沸点:甲>乙b.稳定性:甲>乙,沸点:甲<乙
c.稳定性:甲<乙,沸点:甲<乙d.稳定性:甲<乙,沸点:甲>乙
(3)R元素的气态氢化物丙的沸点比同主族下一周期的元素气态氢化物高很多,原因是:________________________________________________;丙的空间构型________,杂化轨道类型________。
(4)Q、R、X三种元素的第一电离能数值由小至大的顺序为________(用元素符号作答)。
(5)Q的一种氢化物相对分子质量为26,其分子中σ键与π键键数之比为________。