A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去)。
回答下列问题:
(1)若A是非金属单质,X是强氧化性单质,C与水反应生成酸。则X是 ,A可能是 ;
(2)若A是强酸,X是金属单质,向C的水溶液中滴加BaCl2溶液不产生沉淀。则A是 ,X是 ;
(3)若A是一种铁矿石,反应①和②都是工业制硫酸生产中的重要反应,C与水反应生成强酸D。则工业生产中反应①发生的设备名称是 ,铜与D在一定条件下发生反应的方程式是 。
有一瓶无色混和气体,是由HCl、O2、NH3、NO、CO2、N2中的某些气体组成。①把混和气体通过浓硫酸后,气体体积明显减小;② 剩余气体通过碱石灰后,气体体积又明显减小;③ 最后,剩余气体接触空气时,立即变为红棕色。由此可见,原混和气体中,一定含有________________,一定不含__________________(提示: NH3可与H2SO4反应而被吸收,而干燥时与CO2不反应)。
氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40~50 ℃时反应可生成它。CuH具有的性质有:不稳定,易分解;在氯气中能燃烧生成氯化铜和氯化氢;Cu+在酸性条件下发生的反应是2Cu+===Cu2++Cu。与稀盐酸反应能生成一种空气中燃烧火焰为淡蓝色的气体;(提示:CuH中H为-1价)
根据以上信息,结合自己所掌握的化学知识,回答下列问题:
(1)用CuSO4溶液和“另一物质”制CuH的反应中,用氧化还原观点分析,这“另一物质”在反应中作________(填“氧化剂”或“还原剂”)。
(2)写出CuH在氯气中燃烧的化学反应方程式:。
(3)写出CuH溶解在稀盐酸中生成气体的化学方程式:
__________。
(6分)"比较"是化学研究物质性质的基本方法之一,请运用比较法解答下列问题:
已知在一定条件下,过氧化钠几乎可与所有的常见气态非金属氧化物反应。
如:2Na2O2+2CO2=2Na2CO3+O2,Na2O2+CO=Na2CO3。
(1)试分别写出Na2O2与SO2、SO3反应的化学方程式。
。
。
(2)当1 mol SO3参加反应时,转移电子的物质的量为mol。
(3)通过比较可知:在气态非金属氧化物中,当非金属元素处于价时,其氧化物与过氧化钠反应就有O2生成。
某河道两旁有甲、乙两厂。它们排放的工业废水中,共含 K+、Ag+、Cu2+、OH-、Cl-和NO3-六种离子。
(1)甲厂的废水明显呈碱性,故甲厂废水中含有的三种离子分别是、、(填离子符号);
(2)乙厂的废水中含有另外三种离子。如果加一定量(选填:活性炭、硫酸亚铁、铁粉),可以回收其中的金属、、(填写金属元素符号)。
(3)另一种设想是将甲厂和乙厂的废水按适当的比例混合,可以使废水中的、、、(填写离子符号)转化为沉淀。经过滤后的废水主要含(填写化学式),可用作肥料来浇灌农田。
2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。已知1molSO2(g)氧化为1molSO3(g)的ΔH=-99kJ·mol-1。请回答下列问题: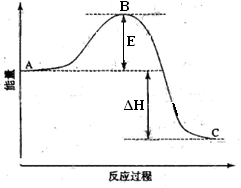
(1)图中A、C分别表示 、 ,E的大小对该反应的反应热 (填“有”或“无”)影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点 (填“升高”还是“降低”),△H (填“变大”、“变小”或“不变”),理由是
(2)图中△H= KJ·mol-1