如图为实验室中常见的气体制备、净化、收集和性质实验的部分仪器,试根据题目要求,回答下列问题: A B C D E F G
A B C D E F G
⑴若以石灰石和稀盐酸为原料制取二氧化碳气体,因盐酸会挥发出少量的氯化氢气体,导致制取的气体不纯,现要收集一瓶干燥、纯净的二氧化碳气体。
①所选仪器的连接顺序为 (填写仪器序号字母)。
②生成二氧化碳时,所发生反应的化学方程式为: 。
③如果仪器F中出现 现象,则证明气体中混有氯化氢气体。
④实验室制取二氧化碳后的剩余废液中,常含有剩余的少量盐酸,欲验证盐酸的存在,请从AgNO3溶液、石蕊、Na2CO3溶液三种试剂中选用一种试剂进行验证,并简述选择的理由 。
⑵若仪器A中盛放Zn和H2SO4溶液,某同学欲利用制备的氢气来测定CuO样品中CuO的纯度(杂质不反应),仪器的连接顺序为A→G→B。(已知:CuO+H2 △ Cu+H2O)
①实验时,会观察到装置G中的黑色固体变成 色。
②该同学通过测量反应前后B装置质量的增加,来计算样品中CuO的纯度,则计算结果会 (填“偏大”、“偏小”、“不受影响”之一)。
有一包白色固体样品,可能是碳酸钠、硫酸钡、氢氧化钠、氯化钡中的一种或几种。为探究其成分,小燕老师取用一定量样品,加足量水溶解,过滤得到白色沉淀甲和无色滤液乙。
写出上述操作中可能发生反应的化学方程式:。
过滤时用到玻璃棒,玻璃棒的作用是。
【探究活动一】 奋进小组探究白色沉淀甲的成分。
| 实验操作 |
实验现象 |
结论 |
| 取白色沉淀甲,滴加足量的稀硝酸 |
沉淀部分消失 |
白色沉淀甲中一定含有 |
【探究活动二】 智慧小组探究白色固体样品中可能含有,设计了如下实验。
| 实验操作 |
实验现象 |
结论 |
|
| 实验Ⅰ |
取适量无色滤液乙,加入碳酸钠溶液 |
无明显现象 |
无色滤液乙中一定不含 |
| 实验Ⅱ |
步骤①:取适量无色滤液乙,加入过量的溶液,过滤 |
生成白色沉淀 |
原白色固体样品中一定存在该物质 |
| 步骤②:取步骤①中的滤液,滴加溶液 |
【反思】 实验Ⅱ中步骤①加入过量试剂的目的是。
【结论】 通过两个小组的共同探究,得出了原白色固体样品含有的成分。
(6分)
做完酸、碱、盐相关性质实验后,某实验小组不小心把稀硫酸、氢氧化钠溶液和碳酸钠溶液混合在一起,看到有大量气泡生成。他们对反应后溶液中溶质的成分很好奇,请你与他们一起进行探究。
【提出问题】反应后溶液中溶质的成为是什么?
【猜想假设】猜想① Na2SO4、Na2CO3猜想② Na2SO4、Na2CO3、NaOH
猜想③ Na2SO4、H2SO4、Na2CO3猜想④ Na2SO4、 H2SO4
猜想⑤ Na2SO4
上述猜想中,你认为不合理的是猜想(填序号)。
【实验探究】(1)甲同学取少量该溶液于试管中,向其中滴加无色酚酞,发现溶液颜色无变化,据此,他认为猜想⑤是正确的。你认为他的结论是(填“合理”或“不合理”)的,理由是。
(2)乙同学向盛有一根生锈的铁钉的试管中加入适量该溶液,过一会儿取出铁钉,用水洗净,观察到铁锈消失,铁钉变得光亮,溶液变黄。该反应的化学方程式是。
【实验结论】根据上述实验探究,你认为猜想(填序号)是正确的。
【拓展应用】工厂与实验室的酸性废水必须处理至中性再排放,这样做的意义是(答一点即可)。
有一种神奇的蜡烛,点燃后任你怎么吹也吹不灭,而且看上去和普通的蜡烛一模一样,
到底是什么玄机能让蜡烛持续燃烧?请你一起参与探究。
【查阅资料】普通蜡烛由石蜡和蜡烛芯制成的,而吹不灭的蜡烛是在蜡烛芯上包裹一层打火石的粉末。打火石是由某种金属掺入少量稀土元素制成的合金,它的着火点只
有150℃。当蜡烛燃烧时,金属并不燃烧;但当蜡烛吹灭后,未冷却的金属接触到氧气就发生燃烧,从而使蜡烛复燃。
【探究与反思】这种蜡烛燃烧时,蜡烛芯里的金属为什么不燃烧?,这种蜡烛也可以熄灭,你采用的方法是。
【实验探究】吹不灭的蜡烛芯内的金属可能是镁、铝、铁或铜中的一种,为确定该金属的成分,请你继续探究并完成下列有关问题:(注:不考虑打火石中稀土元素对探究金属性质的影响)
| 实验 |
操作步骤 |
现象 |
结论 |
| 1 |
切开蜡烛,取出打火石,用砂纸打磨 |
打火石是银白色 |
|
| 2 |
该金属一定不是铁 |
||
| 3 |
取少量打磨后的打火石于试管中,滴加硫酸铜溶液。 |
有红色物质析出 |
该金属一定是镁 |
【分析思考】
(1)请写出“实验3”中可能涉及到的化学方程式。
(2)有同学认为通过“实验3”中现象不能证明烛芯内的金属一定是镁,因为。
(3)针对以上实验,请你设计一个合理的实验方案来进一步验证这种金属,
| 操作步骤 |
现象 |
结论 |
某兴趣小组发现一袋腌制松花蛋的泥料,配料表上的成分是氧化钙、纯碱和食盐。他们要探究在腌制松花蛋过程中都有哪些物质对鸭蛋起作用。于是取少量泥料在水中溶解,充分搅拌后过滤,取滤液探究其成分。
【猜想与假设】他们都认为滤液中一定有NaCl和NaOH。生成氢氧化钠的化学方程式为。对其他成分他们分别做出了如下猜想:
小亮猜想:还可能有Na2CO3
小强猜想:还可能有Ca(OH)2和Na2CO3
你认为谁的猜想是错误的,理由是。你还能做出的猜想是:还可能有。
【活动与探究】小亮取一定量的滤液于试管中,向其中滴加了几滴稀盐酸,振荡,没有气泡,于是他得出结论:没有Na2CO3。
【反思】小强认为小亮的结论不严密,理由是。
(7分) 已知某NH4NO3样品中可能混入了Cu、 CuO、 NH4Cl、 (NH4)2SO4四种物质中的两种或多种。按图所示进行实验,出现的现象如图所示(设过程中所有发生的反应均恰好完全进行)。试根据实验过程和发生的现象填写以下空白: 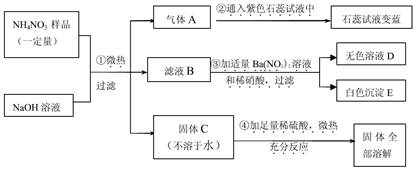
(1)气体 A的化学式是。
(2)样品中一定含有的物质是(写化学式)。
(3)滤液 B 中大量存在的金属离子为(写离子符号)。
(4)写出过程④中发生的一个化学反应方程式。
(5)样品中还不能确定存在的物质是,要进一步证明该物质是否存在,可用溶液D 再实验,请简要说明实验操作步骤、发生的现象及结论:。